题目内容
【题目】高氯酸钾(KClO4)主要用于生产烟花爆竹。以下是工业生产高氯酸钾 的工艺流程图,请回答问题。
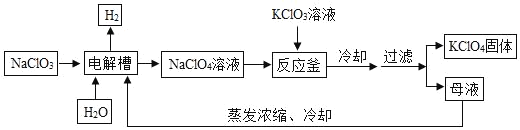
(1)冷却后过滤,说明高氯酸钾的溶解度随温度降低而_____。
(2)母液进入电解槽中需经蒸发浓缩,实验室进行蒸发浓缩时需不停搅拌,其目 的为_____。
(3)反应釜中发生复分解反应,该反应的化学方程式为_____。
(4)流程中可循环利用的物质(除水外)为_____。
【答案】减小 防止受热不均匀而迸溅 KClO3+NaClO4=KClO4↓+NaClO3 NaClO3
【解析】
(1)冷却后过滤,说明降温有晶体析出,即高氯酸钾的溶解度随温度降低而 减小。
(2)母液进入电解槽中需经蒸发浓缩,实验室进行蒸发浓缩时需不停搅拌,其目 的为 防止受热不均匀而迸溅。
(3)反应釜中发生复分解反应,是KClO3和NaClO4生成KClO4和NaClO3,由于图中显示KClO4为固体,所以该反应的化学方程式为 KClO3+NaClO4=KClO4↓+NaClO3。
(4)流程中可循环利用的物质(除水外)为 NaClO3。
故答案为:
(1)减小。(2)防止受热不均匀而迸溅。(3)KClO3+NaClO4=KClO4↓+NaClO3。(4)NaClO3。

【题目】日常生活中,人们利用碳酸钠溶液具有碱性,清洗餐具上的油污,碱性越强,去油污的效果越好。下面实验是影响碳酸钠溶液碱性的因素展开探究。用碳酸钠固体和不同温度的水,配置溶质质量分数分别为 2%、6%和10%的碳酸钠溶液,立即测量溶液的pH,记录如下表:
实验编号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
溶质质量分数 | 2% | 2% | 2% | 6% | 6% | 6% | 10% | 10% | 10% |
水的温度/°C | 20 | 40 | 60 | 20 | 40 | 60 | 20 | 40 | 60 |
溶液 pH | 10.90 | 11.18 | 11.26 | 11.08 | 11.27 | 11.30 | 11.22 | 11.46 | 11.50 |
(1)去油污的效果最好的是___________ (填实验编号)。
(2) 在一定温度范围内,温度对碳酸钠溶液pH的影响是:当_______相同时,______。
(3)如果某实验小组想得到更好的去污效果,根据之前的实验规律,可以尝试的实验条件是__________________
A 12%、 60°C B 8%、 40° C C 10%、 70°C
(4)碳酸钠溶液呈碱性的原因是:一部分碳酸根离子水解产生碳酸氢根离子和氢氧根离子,少部分碳酸氢根离子水解产生碳酸和氢氧根离子。计算100g10%碳酸钠溶液中碳元素的质量是_________g(精确到0.1)