题目内容
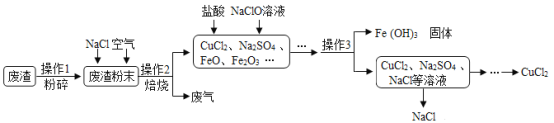
【题目】高纯度的氧化钙是电子工业中的重要原料.用优质的大理石(主要成分是CaCO3)制备高纯度的氧化钙的流程如图:
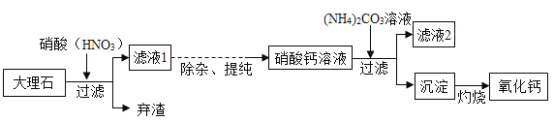
回答下列问题:
(1)大理石与硝酸反应的现象是_________.
(2)加入(NH4)2CO3溶液时发生反应的化学方程式是______________.
(3)将滤液2经过蒸发浓缩、__、过滤,可得到氮肥晶体.
(4)含CaCO3的质量分数90%的大理石1000kg经过上述流程,若不考虑钙元素的损失,理论上可以得到氧化钙__ kg.
【答案】有气泡冒出 ![]() 冷却结晶 504
冷却结晶 504
【解析】
碳酸钙和硝酸反应生成硝酸钙和水和二氧化碳,硝酸钙和碳酸铵反应生成碳酸钙白色沉淀和硝酸铵,将滤液2经过浓缩、冷却结晶、过滤,得到氮肥晶体。
(1)大理石与硝酸反应生成硝酸钙、水和二氧化碳,现象是有气泡冒出。
(2)加入(NH4)2CO3溶液时发生反应是硝酸钙和碳酸铵反应生成碳酸钙白色沉淀和硝酸铵,反应的化学方程式是![]() 。
。
(3)将滤液2经过蒸发浓缩、冷却结晶、过滤,可得到氮肥晶体。
(4)大理石中碳酸钙的质量为![]()
设理论上可以得到氧化钙的质量为x
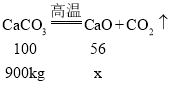
![]()
![]()
含CaCO3的质量分数90%的大理石1000kg经过上述流程,若不考虑钙元素的损失,理论上可以得到氧化钙504kg。

练习册系列答案
相关题目