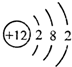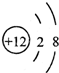题目内容
下列关于空气成分的叙述正确的是
- A.空气中氮气和氧气的体积比约为4:1
- B.空气的成分按质量计算,氮气占78%,氧所占21%
- C.从液态空气中能分离出氮气,不能分离出氧气和稀有气体
- D.空气中含量最多且性质又不活泼的是稀有气体
A
分析:可以根据空气中各种成分的体积含量方面进行分析、判断,从而得出正确的结论.
解答:空气的成分按体积分数计算,大约是氮气为78%、氧气为21%(氮气比氧气约为4:1)、稀有气体为0.94%、二氧化碳为0.03%、其它气体和杂质为0.03%.空气中氮气和氧气的体积比78%:21%≈4:1;液态空气中可以分离出氮气和氧气;空气中含量最多的是氮气,含量稀少的有稀有气体.
故选A
点评:解答本题的关键是要掌握空气的成分及其各种成分的体积分数,只有这样才能对问题做出正确的判断.
分析:可以根据空气中各种成分的体积含量方面进行分析、判断,从而得出正确的结论.
解答:空气的成分按体积分数计算,大约是氮气为78%、氧气为21%(氮气比氧气约为4:1)、稀有气体为0.94%、二氧化碳为0.03%、其它气体和杂质为0.03%.空气中氮气和氧气的体积比78%:21%≈4:1;液态空气中可以分离出氮气和氧气;空气中含量最多的是氮气,含量稀少的有稀有气体.
故选A
点评:解答本题的关键是要掌握空气的成分及其各种成分的体积分数,只有这样才能对问题做出正确的判断.

练习册系列答案
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案
相关题目
(1)如图1,A、B、C三个实验用于验证质量守恒定律:

①实验C中,烧杯中看到的现象是________;
②其中不能达到实验目的是________,理由是________.
(2)如图2是“用木碳还原氧化铜”的演示实验,请回答下列问题:
①写出用木碳还原氧化铜的化学方程式:________;
②反应进行一段时间后,为了探究试管中剩余固体的组成,待试管冷却到室温后,取剩余固体于烧杯中,再加入过量稀硫酸,充分搅拌后过滤.
a.若滤纸上留有黑色、红色固体,而滤液为无色,则滤液中的溶质是________,说明试管中的剩余固体为________;
b.若滤纸上留有黑色、红色固体,而滤液呈蓝色,此时滤液中的溶质是________.
(3)如图是探究酸碱中和的实验:
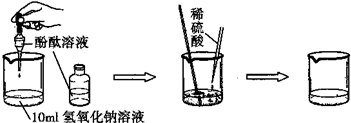
小丽同学为探究上述反应后烧杯中的硫酸是否过量,选取BaCl2、锌粒、紫色石蕊等三种药品和试剂来设计实验,请你根据下表判断出正确的实验方案及分析错误方案的出错原因:
| 实验方案 | 实验步骤 | 实验现象 | 实验结论 |
| 方案一 | 取样,滴入适量的氯化钡溶液 | 出现白色沉淀 | 硫酸过量 |
| 方案二 | 取样,放入几粒锌粒 | 溶液中产生气泡 | 硫酸过量 |
| 方案三 | 取样,滴入几滴紫色石蕊溶液 | 溶液变红 | 硫酸过量 |
②请分析错误方案的原因:________.