题目内容
将二氧化锰放入100g过氧化氢溶液中,至不再有气体生成为止,共收集到氧气0.05mol.
①求参加反应的过氧化氢的质量.(根据化学方程式列式计算)
②该过氧化氢溶液中溶质的质量分数是________.
3.4%
分析:根据化学方程式,已知氧气的物质的量,可求出过氧化氢的物质的量,从而可求出溶液的质量.
解答:设需过氧化氢的物质的量为x,则
2H2O2 2H2O+O2↑
2H2O+O2↑
2 1
x 0.05mol
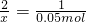
解得:x=0.1mol
①所以过氧化氢的质量为:0.1mol×34g/mol=3.4g
②过氧化氢溶液的质量分数为: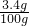 ×100%=3.4%.
×100%=3.4%.
答:①求参加反应的过氧化氢的质量为3.4g;
②该过氧化氢溶液中溶质的质量分数是3.4%.
点评:熟练掌握根据化学方程式计算的一般步骤,并能作出正确的解答,特别注意化学方程式的书写.
分析:根据化学方程式,已知氧气的物质的量,可求出过氧化氢的物质的量,从而可求出溶液的质量.
解答:设需过氧化氢的物质的量为x,则
2H2O2
 2H2O+O2↑
2H2O+O2↑2 1
x 0.05mol
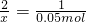
解得:x=0.1mol
①所以过氧化氢的质量为:0.1mol×34g/mol=3.4g
②过氧化氢溶液的质量分数为:
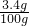 ×100%=3.4%.
×100%=3.4%.答:①求参加反应的过氧化氢的质量为3.4g;
②该过氧化氢溶液中溶质的质量分数是3.4%.
点评:熟练掌握根据化学方程式计算的一般步骤,并能作出正确的解答,特别注意化学方程式的书写.

练习册系列答案
相关题目