题目内容
根据下列粒子的结构示意图,我能回答下列问题:

(1)表示同种元素的粒子是
(2)在化学反应中容易得到电子的粒子是
(3)我国使用“长征三号甲”运载火箭将“嫦娥三号”送上月球,任务之一是研究如何开采月球上丰富的清洁能源氦一3(质子数为2,中子数为1的原子). 氦一3原子核是由一个中子和两个质子构成的,其原子核外电子数为

(1)表示同种元素的粒子是
AD
AD
(填序号);(2)在化学反应中容易得到电子的粒子是
AC
AC
(填序号).(3)我国使用“长征三号甲”运载火箭将“嫦娥三号”送上月球,任务之一是研究如何开采月球上丰富的清洁能源氦一3(质子数为2,中子数为1的原子). 氦一3原子核是由一个中子和两个质子构成的,其原子核外电子数为
2
2
.火箭推进器中盛有联氨液体(N2H4)和过氧化氢(H2O2),当它们混合时产生大量的水蒸气和氮气,并放出大量的热,其反应的化学方程式为N2H4+2H2O2═4H2O+N2↑
N2H4+2H2O2═4H2O+N2↑
.分析:(1)元素是质子数(即核电荷数)相同的一类原子的总称,同种元素的粒子是质子数相同,据此进行分析解答.
(2)若粒子的最外层电子数为8,属于相对稳定结构;若最外层电子数≥4,则一般为非金属元素,在化学反应中易得电子,若最外层电子数<4,则一般为金属元素,在化学反应中易失去电子.
(3)根据原子中:核内质子数=核外电子数;联氨液体(N2H4)和过氧化氢(H2O2)混合时产生大量的水蒸气和氮气,进行分析解答.?
(2)若粒子的最外层电子数为8,属于相对稳定结构;若最外层电子数≥4,则一般为非金属元素,在化学反应中易得电子,若最外层电子数<4,则一般为金属元素,在化学反应中易失去电子.
(3)根据原子中:核内质子数=核外电子数;联氨液体(N2H4)和过氧化氢(H2O2)混合时产生大量的水蒸气和氮气,进行分析解答.?
解答:解:(1)元素是质子数(即核电荷数)相同的一类原子的总称,决定元素种类的是质子数(即核电荷数),同种元素的粒子是质子数相同,AD的质子数相同,属于同种元素.
(2)AC粒子的最外层电子数均是7,大于4,均在化学反应中易得到1个电子而形成阴离子.
(3)由题意,氦-3原子核是由一个中子和两个质子构成的,其核内质子数为2;由原子中:核内质子数=核外电子数,其原子核外电子数为2.
联氨液体(N2H4)和过氧化氢(H2O2)混合时产生大量的水蒸气和氮气,反应的化学方程式为:N2H4+2H2O2═4H2O+N2↑.
故答案为:(1)AD;(2)AC;(3)2;N2H4+2H2O2═4H2O+N2↑.
(2)AC粒子的最外层电子数均是7,大于4,均在化学反应中易得到1个电子而形成阴离子.
(3)由题意,氦-3原子核是由一个中子和两个质子构成的,其核内质子数为2;由原子中:核内质子数=核外电子数,其原子核外电子数为2.
联氨液体(N2H4)和过氧化氢(H2O2)混合时产生大量的水蒸气和氮气,反应的化学方程式为:N2H4+2H2O2═4H2O+N2↑.
故答案为:(1)AD;(2)AC;(3)2;N2H4+2H2O2═4H2O+N2↑.
点评:本题难度不大,考查学生对粒子结构示意图及其意义的理解,了解粒子结构示意图的意义、化学方程式的书写等是正确解题的关键.

练习册系列答案
相关题目



 B:
B: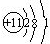 C:
C: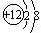 D:
D: E:
E:

