题目内容
向20℃的饱和澄清石灰水(甲溶液)中投入适量的氧化钙粉末,充分反应后,但所得溶液(乙溶液)温度未恢复到20℃.下列说法错误的是( )
| A、乙溶液一定是饱和溶液 | B、乙溶质质量分数比甲溶液大 | C、乙溶液质量比甲溶液小 | D、乙溶液的溶质质量分数和甲溶液的相等 |
分析:解答本题要注意以下几点:
甲溶液为20℃的饱和澄清石灰水,即氢氧化钙饱和溶液;
乙溶液为温度未恢复到20℃的变化后溶液;
氢氧化钙的溶解度随温度升高而逐渐减小,即温度升高氢氧化钙饱和溶液会析出固体氢氧化钙;
氧化钙遇水放出大量热,反应生成氢氧化钙.向溶液中投入氧化钙粉末,溶液中溶剂减少,溶液温度升高.
甲溶液为20℃的饱和澄清石灰水,即氢氧化钙饱和溶液;
乙溶液为温度未恢复到20℃的变化后溶液;
氢氧化钙的溶解度随温度升高而逐渐减小,即温度升高氢氧化钙饱和溶液会析出固体氢氧化钙;
氧化钙遇水放出大量热,反应生成氢氧化钙.向溶液中投入氧化钙粉末,溶液中溶剂减少,溶液温度升高.
解答:解:A、乙溶液是20℃的饱和澄清石灰水经减少水且升高温度所得的溶液,结合氢氧化钙溶解度的特点,升温或减少水都不会改变氢氧化钙饱和溶液的饱和状态.因此乙溶液是饱和溶液的说法正确;
B、乙溶液是升温后温度未恢复到20℃的较高温度下的氢氧化钙饱和溶液,而甲溶液为较低温度20℃时的氢氧化钙饱和溶液,根据氢氧化钙溶解度的特点可以得知,温度越高氢氧化钙溶解度越小,运用饱和溶液的溶质质量分数计算公式:饱和溶液的溶质质量分数=
×100%,可得甲溶液的质量分数大于乙溶液.因此乙溶液质量分数大于甲溶液的说法错误;
C、根据A的分析可以得知,乙溶液质量比甲溶液质量小的说法是正确的;
D、根据B的分析,甲溶液的质量分数大于乙溶液.因此两溶液质量分数相等的说法是错误的.
故选BD
B、乙溶液是升温后温度未恢复到20℃的较高温度下的氢氧化钙饱和溶液,而甲溶液为较低温度20℃时的氢氧化钙饱和溶液,根据氢氧化钙溶解度的特点可以得知,温度越高氢氧化钙溶解度越小,运用饱和溶液的溶质质量分数计算公式:饱和溶液的溶质质量分数=
| 溶解度 |
| 100+溶解度 |
C、根据A的分析可以得知,乙溶液质量比甲溶液质量小的说法是正确的;
D、根据B的分析,甲溶液的质量分数大于乙溶液.因此两溶液质量分数相等的说法是错误的.
故选BD
点评:遇水放出大量热的物质除氧化钙外还有氢氧化钠和浓硫酸,但后两种物质是溶解放热,而氧化钙是与水反应放热.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
向20℃的饱和澄清石灰水(甲溶液)中加入少量氧化钙(CaO)粉末,充分反应.下列对反应后溶液的说法中,错误的是( )
| A、溶液温度未恢复到20℃时,溶液一定是饱和溶液 | B、溶液温度未恢复到20℃时,溶质质量分数比甲溶液的小 | C、溶液温度恢复到20℃时,溶质质量比甲溶液的质量大 | D、溶液温度恢复到20℃时,溶质质量分数与甲溶液的相等 |
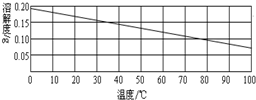 8、图为熟石灰的溶解度曲线.向20℃的饱和澄清石灰水(甲溶液)中加入少量氧化钙(CaO)粉末,充分反应.下列对反应后溶液的说法中,错误的( )
8、图为熟石灰的溶解度曲线.向20℃的饱和澄清石灰水(甲溶液)中加入少量氧化钙(CaO)粉末,充分反应.下列对反应后溶液的说法中,错误的( )