题目内容
【题目】在实验室中,某同学发现了一瓶敞口放置的氢氧化钙粉末试剂,并对其产生兴趣,进行了如下实验。
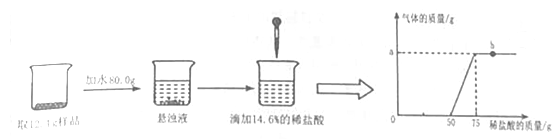
根据实验过程和图象提供的信息,回答下列问题:
(1)完全反应后生成气体的质量是 g。
(2)b点溶液中的溶质为 (填名称)。 _
(3)求恰好完全反应时所得溶液中溶质的质量分数?(利用化学方程式进行计算,书写计算过程,结果精确到0.1%)
【答案】(1)2.2(1分) (2)氯化钙 氯化氢 (1分) (3)10.1%(2分)
【解析】(1)完全反应后生成气体的质量为X
CaCO3+2HCl==CaCl2+H2O+CO2↑
73 44
14.6%×25g X
73/44=( 14.6%×25g )/x
X=2.2g
(2)b点溶液中的溶质为氯化钙和氯化氢;因为盐酸与氢氧化钙和碳酸钙反应完全,生成氯化钙,盐酸过量含有氯化氢气体;
(3)设得到氯化钙的质量为Y
CaCO3+2HCl= =CaCl2+H2O+CO2↑
73 111
14.6%×75g Y
73/111==(14.6%×75g)/y
Y=16.65g
溶液的质量为:12.4g+80g+75g-2.2g=165.2g
恰好完全反应时所得溶液中溶质的质量分数为16.65g÷165.2g×100%=10.1%

练习册系列答案
 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案
相关题目