题目内容
【题目】右图为A、B、C在水中的溶解度曲线图:
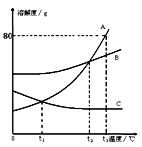
(1)A、C交点的意义是 ;
(2)t3℃时,A、B、C三者的溶解度由大到小的顺序是_________ __;若在该温度时将45克A放入50克水中, 形成的溶液是__ 溶液(填“饱和”或“不饱和”);
(3)如果有A、B的混合物(含少量的B),将A提纯的方法是 ;
(4)t2℃时,等质量的A、B、C三种物质的饱和溶液,温度升高到t3℃,所得溶液溶质质量分数由大到小的顺序是: 。
【答案】(1)t1℃时,甲、乙两物质的溶解度相等
(2)A﹥B﹥C 饱和(3)冷却热饱和溶液(或冷却结晶)(4)A﹦B﹥C
【解析】
试题分析:(1)t1℃时,A、C交点的意义是t1℃时,甲、乙两物质的溶解度相等;
(2)由溶解度曲线可知,t3℃时,A、B、C三者的溶解度由大到小的顺序是A﹥B﹥C;t3℃时,A的溶解度为80g,即该温度时,80gA溶解在100g水中恰好形成饱和溶液,那么将45克A放入50克水中,只能溶解40g,形成的溶液的质量=40g+50g=90g,属饱和溶液;
(3)A的溶解度随温度的变化变化较大,故要提纯A,用到的是降温结晶的方法;
(4)A、B的溶解度随温度的升高而增大,故升温后溶质的质量分数不变,即A=B;C的溶解度随温度的升高而减小,故升温后有晶体析出,溶质的质量分数减小,故所得溶液溶质质量分数由大到小的顺序是A﹦B﹥C 。

【题目】同学们对实验“煅烧石灰石”展开深入探究。资料:石灰石中的杂质高温不分解。
①为证明石灰石已分解,三位同学设计方案如下:
Ⅰ.甲同学按图一进行实验(煤气灯亦能达到石灰石分解的温度),观察到烧杯内壁石灰水变浑浊,写出石灰水发生反应的化学方程式 。

II.乙同学按图二进行试验,观察到B中液体变 色,A实验的作用 。
III.大家认为甲同学的方案不合理,请分析原因 。
IV.丙同学取一块质量为12.5g的石灰石煅烧,并记录有关数据如下表
时间(秒) | 0 | 60 | 120 | 180 | 240 | 300 |
固体质量(克) | 12.5 | 12.3 | 11.2 | 9.2 | 8.1 | 8.1 |
根据上述数据判断, 秒时,已经可以证明石灰石开始分解了。240秒时,石灰石已经完全分解了,理由是 。
②根据丙同学记录的数据,该石灰石分解共生成 克CO2,物质的量为 mol。根据化学方程式列式计算:这块石灰石中含碳酸钙的质量是 克。

