题目内容
【题目】根据下列实验装置图,回答问题:
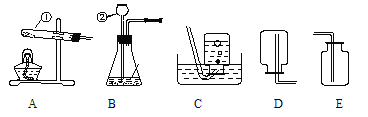
(1)写出标有序号的仪器名称:①__________,② _______;
(2)在实验室中用过氧化氢溶液和二氧化锰混合制取氧气时,其中二氧化锰起____________作用,发生反应的化学方程式为____________;
(3)乙炔是一种无色、无味、密度比空气小,不溶于水的气体;工业上常用它燃烧产生的高温来切割和焊接金属;实验室用电石(固体)与水在常温下反应制乙炔。你认为制取乙炔应选择的装置是________。(填写装置的字母代号)
【答案】 试管 长颈漏斗 催化 略 BC或BD
【解析】【试题分析】
该题是考查学生对制取气体实验的应用(1)根据所给的装置可知,①是试管,②长颈漏斗;(2)实验室用过氧化氢分解制取氧气时,为了加快反应速率,通常加入二氧化锰起催化作用,其反应方程式为 2H2O2![]() 2H2O+O2
2H2O+O2![]() ;(3)制取乙炔是用电石(固体)与水在常温下进行的,不需要加热,故发生装置应选B,乙炔的密度比空气小且难溶于水,可以用排水法或向下排空气法,故可选C或D收集,因此组合装置为BC或BD。
;(3)制取乙炔是用电石(固体)与水在常温下进行的,不需要加热,故发生装置应选B,乙炔的密度比空气小且难溶于水,可以用排水法或向下排空气法,故可选C或D收集,因此组合装置为BC或BD。

 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案【题目】今年春季以来,我国许多城市雾霾天气频发,PM2.5是造成雾霾天气的“元凶”之一。PM2.5是用来监测空气中下列哪项含量的( )
A. 二氧化碳 B. 二氧化氮 C. 可吸入颗粒物 D. 一氧化碳
【题目】氧气在日常生活和T业生产中的用途非常广泛,其实验室的制取是化学研究的重要内容。
(1)根据下列实验装置图回答问题
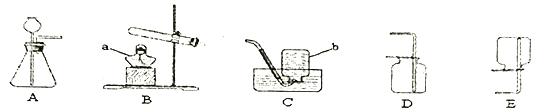
①写出标有字母的仪器名称:a_______ ,b_______ 。
②写出A装置制取O2的化学方程式__________________ 。
③若装置D收集氧气,验满的方法是___________________ 。
(2)实验室常用加热氯酸钾与二氧化锰混合物的方法制取氧气,写出反应的化学方程式:_______ ;
小芳发现,氯酸钾与氧化铜混合加热,也能较快产生氧气,于是进行如下探究:
【提出猜想】除Mn02,Cu0外,Fe2O3,也可以作KC103分解的催化剂。
【实验验证】按下表进行实验:经测定分解温度(分解温度越低,催化效果越好)。
实验编号 | 实验药品 | 分解温度( |
① | KC103 | 580 |
② | KC103、Mn02质量比1:1) | 350 |
③ | KC103,Cu0(质量比1:1) | 370 |
④ | KC103、Fe203(质量比1:1) | 390 |
【分析数据、得出结论】由实验________与实验④对比,证明猜想合理。
【拓展延伸】如果将KMn04固体与KC103固体混合加热,则KC103的分解速率大大加快。请说明KMn04在KCIO3的分解反应中是否作催化剂,为什么?_______________
【实验反思】同种催化剂,颗粒大小可能影响催化效果,请设计实验方案进行验证____________ 。
(3)在实验室中用高锰酸钾制取氧气,若产生9.6克氧气需要分解________克高锰酸钾?