题目内容
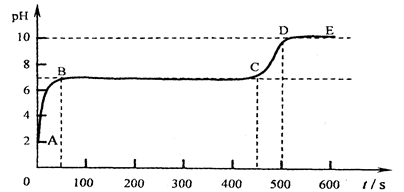
下列图象对应叙述关系正确的是

A B C D
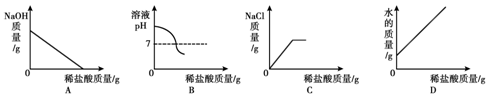
| A.向pH=3的溶液中加水 | B.一定质量的稀盐酸与锌粒反应 |
| C.向H2SO4和CuSO4混合溶液中加NaOH溶液 | D.煅烧一定质量的石灰石 |

A B C D
C
A、向pH=3的溶液中不断加水,酸性会减弱,pH会增大,但不能超过7,故此选项错误.
B、随着反应的进行,氢气质量增加,当稀硫酸完全反应时,氢气的质量不再增加,故此选项错误.
C、该过程先发生酸碱中和,酸完全反应后,NaOH再与CuSO4反应,才出现沉淀;故此选项正确.
D、煅烧一定质量的石灰石,固体剩余物是氧化钙和杂质,固体的质量不能是零,故此选项错误.
故选C.
B、随着反应的进行,氢气质量增加,当稀硫酸完全反应时,氢气的质量不再增加,故此选项错误.
C、该过程先发生酸碱中和,酸完全反应后,NaOH再与CuSO4反应,才出现沉淀;故此选项正确.
D、煅烧一定质量的石灰石,固体剩余物是氧化钙和杂质,固体的质量不能是零,故此选项错误.
故选C.

练习册系列答案
相关题目