题目内容
【题目】Ⅰ.日常生活中化学无处不在,从石墨、二氧化硫、熟石灰、醋酸、碳酸氢铵等物质中,选择与下列叙述相应的物质,用化学式填空:
(1)可用作建筑材料的是 .
(2)形成酸雨的主要气体是 .
(3)可用于制铅笔芯的是 .
(4)农业上可用作化肥的是 .
(5)可用于清洗热水瓶内壁水垢的是 .
(6)Ⅱ.如图是元素周期表部分内容,请根据表中信息完成相关问题.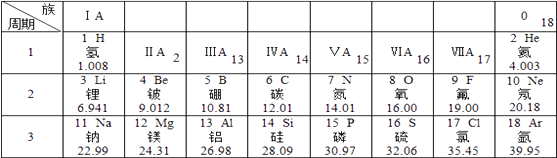
铍原子的相对原子质量是 , 它属于(填“金属”或“非金属”)元素.
(7)不同种元素最本质的区别是 .
(8)原子序数为1、6、8的三种元素形成的常见化合物的化学式为 , 其中6号元素的化合价是 .
【答案】
(1)Ca(OH)2
(2)SO2
(3)C
(4)NH4HCO3
(5)CH3COOH
(6)9.012,金属
(7)核内质子数不同
(8)H2CO3,+4
【解析】(1)熟石灰能与二氧化碳反应生成碳酸钙,可用作建筑材料,氢氧化钙表示为Ca(OH)2;
(2)二氧化硫是形成酸雨的主要气体,二氧化硫表示为SO2;
(3)石墨很软,可用于制铅笔芯,石墨是由碳元素组成的单质,表示为C;(4)碳酸氢铵是常用的氮肥,碳酸氢铵表示为NH4HCO3;
(5)水垢的主要成分是碳酸钙,可用醋酸清洗,醋酸表示为CH3COOH;
(6)元素名称下面的数字表示的是相对原子质量,故铍原子的相对原子质量是9.012,由元素的名称可知铍元素属金属元素;
(7)元素是具有相同核电荷数或质子数的同一类原子的总称,故不同种元素最本质的区别是质子数不同;
(8)原子序数为1、6、8分别是氢元素、碳元素和氧元素,这三种元素可组成碳酸,碳酸表示为H2CO3;氢元素为+1价,氧元素为-2价,根据“在化合物中,正负化合价的代数和为零”的原则,设碳元素的化合价为x,那么(+1)×2+x+(-2)×3=0,解得x=+4 .
所以答案是:(1)Ca(OH)2;(2)SO2;(3)C;(4)NH4HCO3;(5)CH3COOH;(6)9.012;金属;(7)核内质子数不同;(8)H2CO3;+4.

 阅读快车系列答案
阅读快车系列答案【题目】某研究小组对自动充气气球(示意图如图)进行下列探究.
[查阅资料]该气球充气原理是:通过挤破液体包,使液体与白色粉末接触产生二氧化碳气体,实现气球自动充气.
(1)为检验气体是二氧化碳,可选用(填试剂名称).
(2)探究一:液体包内溶液酸碱性的探究
室温时,用pH试纸测得溶液的pH=3,则该溶液呈性.
(3)探究二:白色粉末成分的探究
[猜想与假设]甲同学认为是碳酸钙;乙同学认为是碳酸钠;丙同学认为是碳酸氢钠.
[设计并进行实验]
将少量白色粉末放入水中搅拌,固体全部溶解,说明甲同学的猜想(填“正确”或“不正确”).
(4)室温时,分别向盛有碳酸氢钠、碳酸钠和白色粉末样品的锥形瓶中注入等体积、足量的10%盐酸(装置如图2),记录如表:
实验编号 | 锥形瓶内物质 | 最终得到CO2体积/mL | |
名称 | 质量/g | ||
① | 碳酸氢钠 | 0.10 | V1 |
② | 碳酸钠 | 0.10 | V2 |
③ | 白色粉末 | a | V1 |

实验①的化学方程式为;表中a=;V1V2(填“>”、“<”或“=”).
[分析并得出结论]
根据表中CO2体积与锥形瓶内物质质量的关系,实验③与实验①相同,可得出白色粉末的成分为碳酸氢钠。