题目内容
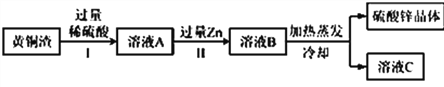
【题目】为了达到收旧利废节能减排的目的,从含有金属镁、铁、铜的粉末中,分离和提取出重要化工原料MgSO4和有关金属,实验过程如下:

请回答:
(1)操作a的名称是_____________________;在此过程中需要使用玻璃棒,其作用是_____________________.
(2)写出步骤②所涉及的化学反应方程式 ____________________。
【答案】 过滤 引流 Mn+H2SO4=MnSO4+H2↑
【解析】(1)经过操作a可以得到固体金属B和溶液,故该操作为过滤,玻璃棒的作用是引流;(2)加入适量的稀硫酸,镁与硫酸反应,铜不反应,因此“过滤”可以得到B,即金属铜;镁和硫酸反应生成硫酸镁和氢气,其化学方程式为: ![]() 。
。

练习册系列答案
 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案
相关题目
【题目】亮亮做家务时接触到下列用品。
用品 | 脱氧剂 | 洁厕灵 | 炉灶清洁剂 |
有效成分 | 还原铁粉 | 盐酸 | 氢氧化钠 |
(1)他清理垃圾时发现一袋脱氧剂,拆开后看到还原铁粉已生锈,为检验铁粉是否还有效,可向其中滴加盐酸,若看到_____现象,说明还有效。
(2)他清洗炉灶时戴上橡胶手套,以防清洁剂与皮肤直接接触,其原因是_____。