题目内容
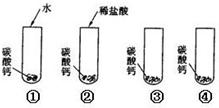
(2009?长沙)碳酸钙是一种白色固体,可溶于稀盐酸并产生无色气体.某同学想知道稀盐酸中的哪种粒子(H2O、H+、Cl-)能使碳酸钙溶解并产生无色气体.请你和他一起通过如图所示的四个实验完成这次探究话动.
(1)你提出的假设是
(2)通过实验①可以证明
(3)要证明另外两种粒子能否溶解碳酸钙并产生无色气体,还需要进行实验③和④:在③中应加入
(4)你的探究结果为

(1)你提出的假设是
稀盐酸中的H+使CaCO3溶解并产生无色气体
稀盐酸中的H+使CaCO3溶解并产生无色气体
.(2)通过实验①可以证明
H2O不能使CaCO3溶解并产生无色气体
H2O不能使CaCO3溶解并产生无色气体
.(3)要证明另外两种粒子能否溶解碳酸钙并产生无色气体,还需要进行实验③和④:在③中应加入
硝酸
硝酸
;在④应加入氯化钠溶液
氯化钠溶液
.(4)你的探究结果为
H+使CaCO3溶解并产生无色气体
H+使CaCO3溶解并产生无色气体
.分析:碳酸钙能与盐酸反应生成二氧化碳气体,要探究是稀盐酸中的哪种粒子(H2O、H+、Cl-)能使碳酸钙溶解并产生无色气体,需排除一些离子的干扰,设计实验时要注意控制变量.
解答:解:(1)碳酸盐遇酸化气,是与酸中的氢离子结合反应生成了二氧化碳,所以本题答案为:稀盐酸中的H+使CaCO3溶解并产生无色气体;
(2)向①中加水,碳酸钙不溶解也无气体产生,说明通过实验①H2O不能使CaCO3溶解并产生无色气体,所以本题答案为:H2O不能使CaCO3溶解并产生无色气体;
(3)要证明是否是氢离子使碳酸钙溶解并产生气体,需加入含氢离子的物质,如硝酸,要证明是否是氯离子使碳酸钙溶解并产生气体,需加入含氯离子的物质,如氯化钠溶液,所以本题答案为:硝酸,氯化钠溶液;
(4)根据实验现象,可知是氢离子使碳酸钙溶解并产生气体,所以本题答案为:H+使CaCO3溶解并产生无色气体.
(2)向①中加水,碳酸钙不溶解也无气体产生,说明通过实验①H2O不能使CaCO3溶解并产生无色气体,所以本题答案为:H2O不能使CaCO3溶解并产生无色气体;
(3)要证明是否是氢离子使碳酸钙溶解并产生气体,需加入含氢离子的物质,如硝酸,要证明是否是氯离子使碳酸钙溶解并产生气体,需加入含氯离子的物质,如氯化钠溶液,所以本题答案为:硝酸,氯化钠溶液;
(4)根据实验现象,可知是氢离子使碳酸钙溶解并产生气体,所以本题答案为:H+使CaCO3溶解并产生无色气体.
点评:本题考查了碳酸钙与酸反应的实质,完成此题,要注意设计实验时变量的控制以及归纳法的应用.

练习册系列答案
相关题目