题目内容
(2011?广东模拟)某实验小组的同学对实验室久置的烧碱样品进行分析其变质程度,他们先称取13.3克的烧碱样品,配成溶液,然后向溶液中逐滴加入一定质量分数的稀盐酸,实验测得加入稀盐酸的质量与产生气体的质量关系如图所示:求:(1)该图象中开始一段时间没有气体产生的原因______
(2)样品中碳酸钠的质量分数
(3)所用稀盐酸的溶质质量分数.
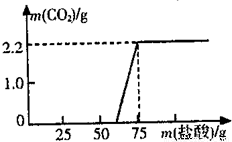
【答案】分析:(1)分析图象可知,刚开始一段时间虽然加入了盐酸,但是没有生成二氧化碳气体,说明盐酸和其他物质(烧碱)发生了反应.
(2)从图象可以看出,加入盐酸总共生成二氧化碳的质量是2.2克,写出化学方程式并代入数据计算碳酸钠的质量.
(3)通过(2)计算出氯化氢的质量(和碳酸钠反应),然后再写出烧碱和盐酸反应的化学方程式,代入烧碱的质量计算出氯化氢的质量(和烧碱反应),两部分氯化氢质量之和就是75克盐酸溶液的溶质.
解答:解:(1)分析图象可知,刚开始一段时间虽然加入了盐酸,但是没有生成二氧化碳气体,说明盐酸和其他物质(烧碱)发生了反应,故答案为:盐酸和烧碱发生中和反应.
(2)从图象可以看出,加入盐酸总共生成二氧化碳的质量是2.2克,设碳酸钠的质量是X,氯化氢的质量为Y.
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 73 44
X Y 2.2克
 ═
═
得:X=5.3克
 ═
═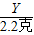
得:Y=3.65克
∴样品中碳酸钠的质量分数= ×100%═39.85%.
×100%═39.85%.
(3)样品中烧碱的质量=13.3克-5.3克=8克,设和烧碱反应的氯化氢的质量是Z.
NaOH+HCl═NaCl+H2O
40 36.5
8克 Z
 ═
═
得Z=7.3克
∴总的氯化氢的质量=7.3克+3.65克=10.95克,根据图象可知,总的盐酸质量是75克.
∴稀盐酸的溶质质量分数= ×100%═14.6%.
×100%═14.6%.
答:样品中碳酸钠的质量分数为39.85%,所用稀盐酸的溶质质量分数为14.6%.
点评:培养学生的看图能力,能够判断二氧化碳的质量和反应的过程,注意计算的格式和规范.
(2)从图象可以看出,加入盐酸总共生成二氧化碳的质量是2.2克,写出化学方程式并代入数据计算碳酸钠的质量.
(3)通过(2)计算出氯化氢的质量(和碳酸钠反应),然后再写出烧碱和盐酸反应的化学方程式,代入烧碱的质量计算出氯化氢的质量(和烧碱反应),两部分氯化氢质量之和就是75克盐酸溶液的溶质.
解答:解:(1)分析图象可知,刚开始一段时间虽然加入了盐酸,但是没有生成二氧化碳气体,说明盐酸和其他物质(烧碱)发生了反应,故答案为:盐酸和烧碱发生中和反应.
(2)从图象可以看出,加入盐酸总共生成二氧化碳的质量是2.2克,设碳酸钠的质量是X,氯化氢的质量为Y.
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 73 44
X Y 2.2克
 ═
═
得:X=5.3克
 ═
═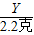
得:Y=3.65克
∴样品中碳酸钠的质量分数=
 ×100%═39.85%.
×100%═39.85%.(3)样品中烧碱的质量=13.3克-5.3克=8克,设和烧碱反应的氯化氢的质量是Z.
NaOH+HCl═NaCl+H2O
40 36.5
8克 Z
 ═
═
得Z=7.3克
∴总的氯化氢的质量=7.3克+3.65克=10.95克,根据图象可知,总的盐酸质量是75克.
∴稀盐酸的溶质质量分数=
 ×100%═14.6%.
×100%═14.6%.答:样品中碳酸钠的质量分数为39.85%,所用稀盐酸的溶质质量分数为14.6%.
点评:培养学生的看图能力,能够判断二氧化碳的质量和反应的过程,注意计算的格式和规范.

练习册系列答案
相关题目
 金属混合物+溶液A
金属混合物+溶液A Ag+溶液B(B中溶质有三种元素组成)
Ag+溶液B(B中溶质有三种元素组成)