题目内容
如图为干电池的结构示意图,请利用所学知识完成下列问题。

(l)碳棒(主要成分是石墨)可用作干电池的电极,说明石墨具有_____________性。
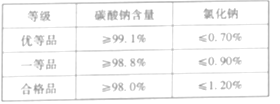
(2)把NH4Cl配制成溶液,并结合下表填空。
①通过观察上表可知,NH4Cl溶液的 pH___________(填“>”“<”或者“=”)7。
②上表中属于碱性氮肥的是____________。
(3)干电池中用到了铜和锌两种金属,请你写出一种证明两种金属活动性强弱的方案,(写操作和现象)___________。
溶液 | K2SO4 溶液 | NH4Cl 溶液 | 氨水 | K2CO3 溶液 |
加入紫色石蕊溶液 | 紫色 | 红色 | 蓝色 | 蓝色 |
(4)干电池的材料很多可以回收利用。例如:回收的二氧化锰在实验室制取氧气时,所起的作用是 _____________; 干电池中的锌壳可以回收用于实验室制取氢气,反应的化学方程式为___________。
练习册系列答案
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案
相关题目
为达到以下实验目的所设计的实验方案,不合理的是( )
实验目的 | 实验方案 | |
A | 区别NaCl、Na2CO3两种溶液 | 滴加酚酞试剂 |
B | 鉴别某种溶液是FeCl2溶液 | 观察溶液颜色,滴加AgNO3溶液 |
C | 除去NaCl溶液中的Na2SO4 | 滴加适量BaCl2溶液,充分反应后,过滤 |
D | 分离出含有少量NaCl的KNO3 | 高温下配制KNO3的饱和溶液,趁热过滤 |
A. A B. B C. C D. D



 B. 通入少量CO2
B. 通入少量CO2
 D. 放入冰水中
D. 放入冰水中
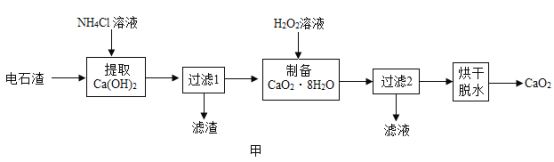
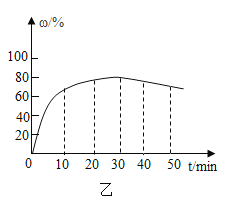
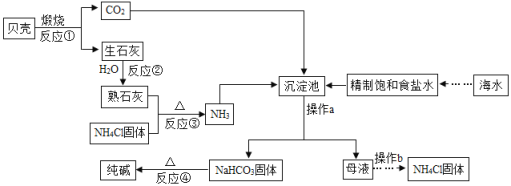
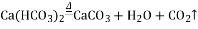 ,Ca(HCO3)2和NaHCO3化学性质相似。写出反应④的化学方程式:___________;请列举小苏打在生活中的一种常见用途_________。
,Ca(HCO3)2和NaHCO3化学性质相似。写出反应④的化学方程式:___________;请列举小苏打在生活中的一种常见用途_________。