题目内容
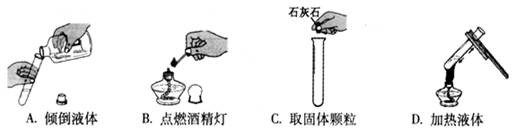
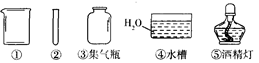
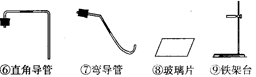
(6分)图15是实验室制备气体常用的装置图,请按要求填空。
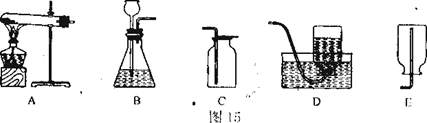
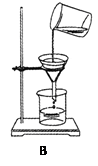
(1)写出B装置中两种仪器的名称:__________、_____________。
(2)实验室用5%的双氧水溶液在MnO2存在的条件下制氧气,应选择的发生装置为_______(填字母),该装置还可用来制取________(填一种物质的化学式)气体。
(3)根据反应2NH4Cl(固)+Ca(OH)2(固) CaCl2+2NH3↑十+2H2O制取氨气,已知氨气密度比空气小,且易溶于水,则发生装置用___________(填字母,下同),收集装置选用_________。
CaCl2+2NH3↑十+2H2O制取氨气,已知氨气密度比空气小,且易溶于水,则发生装置用___________(填字母,下同),收集装置选用_________。
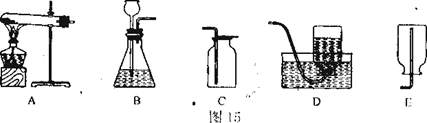
(1)写出B装置中两种仪器的名称:__________、_____________。
(2)实验室用5%的双氧水溶液在MnO2存在的条件下制氧气,应选择的发生装置为_______(填字母),该装置还可用来制取________(填一种物质的化学式)气体。
(3)根据反应2NH4Cl(固)+Ca(OH)2(固)
 CaCl2+2NH3↑十+2H2O制取氨气,已知氨气密度比空气小,且易溶于水,则发生装置用___________(填字母,下同),收集装置选用_________。
CaCl2+2NH3↑十+2H2O制取氨气,已知氨气密度比空气小,且易溶于水,则发生装置用___________(填字母,下同),收集装置选用_________。(1)长颈漏斗锥形瓶(或其他合理答案)
(2)B CO2 (3)A E
(2)B CO2 (3)A E
分析:(1)由装置图中仪器的图示,写出该装置中所使用的仪器名称;
(2)由实验室用5%的双氧水溶液在MnO2存在的条件下制氧气的反应特点,判断可用于该反应的发生装置,并由该发生装置的特点判断使用该装置还可以制取的气体;
(3)由题中所提供制取氨气的反应化学方程式,分析反应的特点从而判断可用于该反应的发生装置,结合氨气密度及溶解性判断收集氨气的方法.
解答:解:(1)装置B由加入液体的仪器长颈漏斗、反应容器锥形瓶和导管所组成;
(2)用5%的双氧水溶液在MnO2存在的条件下制氧气,反应为固体二氧化锰与液体过氧化氢在常温下进行,因此发生装置应选用适用于固体与液体在常温下发生反应的装置B;该装置还可用于固体大理石与稀盐酸反应制取二氧化碳、锌粒与稀硫酸反应制取氢气;、
(3)根据制取氨气反应的化学方程式2NH4Cl(固)+Ca(OH)2(固) CaCl2+2NH3↑十+2H2O,可知通过加热氯化铵与氢氧化钙的固体混合物制取氨气,因此发生装置应选用可用于对固体加热的装置A;由于氨气密度比空气小,且易溶于水,因此只能采取向下排空气法即装置E收集氨气.
CaCl2+2NH3↑十+2H2O,可知通过加热氯化铵与氢氧化钙的固体混合物制取氨气,因此发生装置应选用可用于对固体加热的装置A;由于氨气密度比空气小,且易溶于水,因此只能采取向下排空气法即装置E收集氨气.
故答案为:
(1)长颈漏斗,锥形瓶;
(2)B,CO2;
(3)A,E.
点评:解答此题的关键是要明白实验室制取气体时,应该根据反应物的状态和反应的条件选择需要什么样的发生装置;根据制取气体的溶解性和密度的大小选择收集气体的方法
(2)由实验室用5%的双氧水溶液在MnO2存在的条件下制氧气的反应特点,判断可用于该反应的发生装置,并由该发生装置的特点判断使用该装置还可以制取的气体;
(3)由题中所提供制取氨气的反应化学方程式,分析反应的特点从而判断可用于该反应的发生装置,结合氨气密度及溶解性判断收集氨气的方法.
解答:解:(1)装置B由加入液体的仪器长颈漏斗、反应容器锥形瓶和导管所组成;
(2)用5%的双氧水溶液在MnO2存在的条件下制氧气,反应为固体二氧化锰与液体过氧化氢在常温下进行,因此发生装置应选用适用于固体与液体在常温下发生反应的装置B;该装置还可用于固体大理石与稀盐酸反应制取二氧化碳、锌粒与稀硫酸反应制取氢气;、
(3)根据制取氨气反应的化学方程式2NH4Cl(固)+Ca(OH)2(固)
 CaCl2+2NH3↑十+2H2O,可知通过加热氯化铵与氢氧化钙的固体混合物制取氨气,因此发生装置应选用可用于对固体加热的装置A;由于氨气密度比空气小,且易溶于水,因此只能采取向下排空气法即装置E收集氨气.
CaCl2+2NH3↑十+2H2O,可知通过加热氯化铵与氢氧化钙的固体混合物制取氨气,因此发生装置应选用可用于对固体加热的装置A;由于氨气密度比空气小,且易溶于水,因此只能采取向下排空气法即装置E收集氨气.故答案为:
(1)长颈漏斗,锥形瓶;
(2)B,CO2;
(3)A,E.
点评:解答此题的关键是要明白实验室制取气体时,应该根据反应物的状态和反应的条件选择需要什么样的发生装置;根据制取气体的溶解性和密度的大小选择收集气体的方法

练习册系列答案
 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案
相关题目