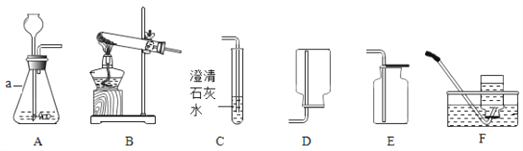
题目内容
【题目】现将石灰石样品15g与过量的105.4g稀盐酸放入烧杯中充分反应(杂质不与稀盐酸反应),反应时间与反应前后烧杯内物质的质量变化如表所示:
反应时间/s | 20 | 40 | 60 | 80 | 100 | 120 |
质量/g | 119.52 | 118.64 | 117.76 | 116.88 | 116 | 116 |
请回答:
(1)完全反应后生成CO2的质量是___g。
(2)计算样品中碳酸钙的质量分数为多少?(计算结果保留一位小数)
【答案】(1)4.4;(2)66.7%
【解析】(1)碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,当烧杯中的物质的质量不再坚守时,表示碳酸钙与稀盐酸反应完全,生成的二氧化碳的质量=15g+105.4g-116g=4.4g;
(2)利用化学方程式,根据碳酸钙与二氧化碳反应的质量比即可计算出碳酸钙的质量。
CaCO3 + 2HCl == CaCl2 + H2O + CO2↑
100 44
X 4.4g
![]() x=10g
x=10g
样品中碳酸钙的质量分数=![]() 66.7%
66.7%
答:样品中碳酸钙的质量分数为66.7% 。

 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案【题目】为探究氢氧化钙溶液和稀盐酸反应所得溶液中溶质的成分,小鸣和同学们通过测定了反应后溶液的pH,得到了如下图所示的pH曲线,请回答:
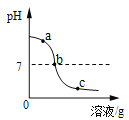
(1)由图可知该实验操作是将__________滴加到另一种溶液中;
(2)该反应的化学方程式为___________;
(3)实验过程中,小鸣取了a、b、c三处反应后的溶液于三个烧杯中,却忘了作标记,请你设计不同的方案(不再用测定pH的方法),探究三种样品分别属于哪处溶液。
【查阅资料】CaCl2溶液显中性,CaCl2+Na2CO3=CaCO3↓+2NaCl。
【探究过程】
①分别取少量样品于三支试管中,加入酚酞试液,观察到其中一支试管内出现___________的现象。结论:该样品是a处溶液。
②为进一步确定b或c处溶液,又设计了以下方案:
实验步骤 | 实验现象 | 实验结论 |
另取余下样品少量于两支试管中,分别滴加足量的Na2CO3溶液。 | ________ | 该样品为b处溶液。 |
【反思评价】探究反应后溶液中溶质的成分,除了要考虑生成物之外,还要考虑____________。
【题目】下图是某燃气热水器的内部构造示意图。
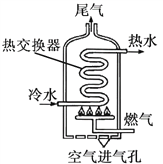
(1)热值是指1kg某种燃料完全燃烧放出的热量,常见三种燃料的热值及1kg燃料燃烧产生的CO2和SO2的质量如下表。
燃料 | 热值kJ/kg | 燃烧产物的质量/g | |
二氧化碳 | 二氧化硫 | ||
汽油 | 约48000 | 2900 | 5.0 |
天然气 | 约56000 | 2500 | 0.1 |
煤 | 约33000 | 2500 | 11.0 |
结合上表数据分析:以上三种燃料中最清洁高效的能源是______,理由是______。
(2)当“空气进气孔”部分堵塞,燃料不完全燃烧时产生有毒的__气体;燃气热水器中的热交换器采用了回形管结构,它的优点是______。