题目内容
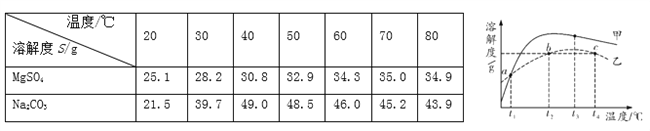
【题目】下图是甲、乙、丙三种物质的溶解度曲线。下列叙述正确的是( )
A.升高丙溶液的温度,一定有晶体析出
B.在t3℃时,分别制成甲、乙的饱和溶液,乙中溶质质量比甲中的小
C.组成为N点的甲溶液可通过增加溶质或恒温蒸发水变为M点的溶液
D.将t3℃时的甲、乙、丙三种物质的饱和溶液降温到t2℃,这三种溶液的溶质质量分数的大小关系是乙>甲=丙
【答案】C
【解析】A、在溶解度曲线图上,横坐标是温度,纵坐标是溶解度。溶解度是一定温度下,100g溶剂里达到饱和时,所溶解的溶质的质量。饱和溶液是在一定温度下、一定量的溶剂里不能再溶解某物质的溶液叫该物质的饱和溶液,反之为不饱和溶液。由图知,丙的溶解度随温度的升高而减小,所以将丙的饱和溶液升温时会有晶体析出;
B. 在t3℃时,分别制成等质量的甲、乙的饱和溶液,乙中溶质质量比甲中的小;
C. M点和N点溶剂的质量相等,M中溶质的质量比N点溶质多,即M点溶液的质量分数比N的大,所以组成为N点的甲溶液可通过增加溶质或恒温蒸发水变为M点的溶液;
D. 饱和溶液溶质的质量分数=溶解度÷(溶解度+100g)×100% ,将t3℃时的甲、乙、丙三种物质的饱和溶液降温到t2℃,甲乙的溶解度减小,析出晶体,得t2℃时的饱和溶液,t2℃时,乙的溶解度大于甲的溶解度,质量分数乙>甲;降温时丙的溶解度增大,溶质的质量等于t3℃时的溶解度,而丙t3℃时的溶解度小于t2℃时甲的溶解度,这三种溶液的溶质质量分数的大小关系是乙>甲>丙.
所以答案是:C.
【考点精析】利用饱和溶液和不饱和溶液相互转变的方法和固体溶解度曲线及其作用对题目进行判断即可得到答案,需要熟知饱和和不饱和的转变方法:①Ca(OH)2和气体等除外,它的溶解度随温度升高而降低②最可靠的方法是:加溶质、蒸发溶剂;1.查找指定温度时物质的溶解度,并根据溶解度判断溶解性.2.比较相同温度时(或一定温度范围内)不同物质溶解度的大小.3.比较和确定物质的溶解度受温度影响的程度,并据此确定物质结晶或混合物分离提纯的方法.4.确定溶液的状态(饱和与不饱和).

 天天向上一本好卷系列答案
天天向上一本好卷系列答案