题目内容
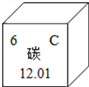
【题目】在煤中加入适量的生石灰(主要成分为CaO)制成供居民采暖用的“环保煤”,可以减少二氧化硫的排放,减弱二氧化硫对空气的污染。“环保煤”燃烧时,生石灰吸收二氧化硫的化学方程式为:2CaO+2SO2+mO2 = nCaSO4。请回答下列问题:
(1)m值是___;
(2)若向煤中加入50t含杂质(杂质不参与反应)为20%的生石灰,则理论上最多可吸收二氧化硫_________吨?(计算结果保留一位小数)
【答案】m=1 45.7t
【解析】
由质量守恒定律可得,反应前有2个钙原子,故n=2,可知,反应后氧原子的个数为8个,反应前氧化钙和二氧化硫中共有氧原子6个,故m=1;
解:设50t含杂质(杂质不参与反应)为20%的生石灰,理论上最多可吸收二氧化硫的质量为x,50t样品中生石灰的质量=50t![]() =40t。
=40t。
2CaO+2SO2+O2 = 2CaSO4
112 128
40t x
![]() =
=![]() 解得x=45.7t
解得x=45.7t
答:理论上最多可吸收二氧化硫的质量为45.7t。

练习册系列答案
相关题目