题目内容
13.写出下列反应的化学方程式:(1)二氧化碳和水反应CO2+H2O═H2CO3;
(2)电解水2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;
(3)过氧化氢制氧气2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(4)黑火药是我国古代四大发明之一,它是由硝石(KNO3)、木炭、硫粉组成,点燃后生成硫化钾(K2S)、二氧化碳和一气体单质,并产生猛烈地爆炸威力.2KNO3+S+3C$\frac{\underline{\;点燃\;}}{\;}$K2S+3CO2↑+N2↑.
分析 首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤(写、配、注、等)进行书写即可.
解答 解:(1)二氧化碳和水反应生成碳酸,反应的化学方程式为:CO2+H2O═H2CO3.
(2)水通电分解生成氢气和氧气,反应的化学方程式为:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.
(3)过氧化氢在二氧化锰的催化作用下生成水和氧气,反应的化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
(4)硝石(KNO3)、木炭、硫粉点燃后生成硫化钾(K2S)、二氧化碳和一气体单质(由质量守恒定律,反应前后元素种类不变,该单质为氮气),反应的化学方程式为:2KNO3+S+3C$\frac{\underline{\;点燃\;}}{\;}$K2S+3CO2↑+N2↑.
故答案为:(1)CO2+H2O═H2CO3;(2)2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;(3)2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;(4)2KNO3+S+3C$\frac{\underline{\;点燃\;}}{\;}$K2S+3CO2↑+N2↑.
点评 本题难度不大,考查学生根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
4.根据所学知识,我们可以从“电解水实验”中获得更多的信息和推论.下列说法正确的是( )
| A. | 水是由氢分子和氧分子构成的 | |
| B. | 水是由氢原子和氧原子直接构成的 | |
| C. | 生成的氧气与氢气的质量比约为1:2 | |
| D. | 水是由氢元素和氧元素组成的 |
1.下列物质中,属于氧化物的是( )
| A. | 食用醋 | B. | 氧化镁 | C. | 冰红茶 | D. | 加碘盐 |
18.将25g20%氯化钾溶液稀释到50g,稀释后所得溶液中溶质的质量分数是( )
| A. | 1% | B. | 5% | C. | 10% | D. | 20% |
5.化学兴趣小组的同学对蜡烛(主要成分是石蜡)及其燃烧进行了如下探究.
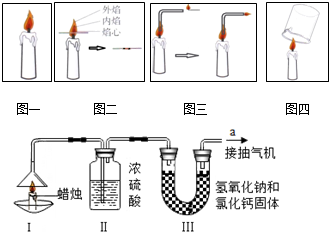
(1)取一支红色的短蜡烛,用小刀切下一小块,把它放入水中,蜡烛一直浮在水面上.据此请总结出常温下蜡烛的两条物理性质:红色固体;不溶于水;密度比水小
(2)点燃蜡烛(图一),能观察到发生化学变化的现象:发光、发热、燃烧等.(写出一条)
(3)取一小木条,迅速平放入火焰中(图二)约一秒后取出,观察到木条表面出现环形焦斑.据此推测,蜡烛火焰中外焰温度最高.
(4)将短玻璃管插入焰心,用燃烧的木条靠近导管另一端(图三),发现导出的气体可以点燃.请你推测导管里气体可能会是石蜡蒸汽.
(5)取一只冷而干燥的小烧杯罩在蜡烛火焰上方(图四),观察烧杯壁上有水珠出现.片刻后取下烧杯,迅速向烧杯中倒入少量澄清的石灰水,振荡,观察到石灰水变浑浊.
据此小明得出蜡烛是由碳、氢元素组成的.你认为他的结论是否正确?不正确.
(6)为了测定蜡烛中碳、氢两 种元素的质量比,小华设计了如图所示的实验.
实验步骤如下:
先分别称量蜡烛、装置Ⅱ(吸收水)、装置Ⅲ(吸收二氧化碳)的质量.按图示连接好仪器,点燃蜡烛,同时从a导管口抽气.一段时间后熄灭蜡烛,再分别称量蜡烛、装置Ⅱ、装置Ⅲ的质量.
实验数据如上表.请回答:
①该实验中测得水的质量为1.8g.
②由该实验数据计算,蜡烛中碳、氢元素的质量之比为6:1.
③理论上,装置Ⅱ和装置Ⅲ增加的总质量大于蜡烛失去的质量,其原因是与消耗的蜡烛比较,生成的二氧化碳和水中增加了参加反应的氧气所含氧元素质量.
④该实验能否准确测出蜡烛燃烧生成二氧化碳和水的质量?说明理由.

(1)取一支红色的短蜡烛,用小刀切下一小块,把它放入水中,蜡烛一直浮在水面上.据此请总结出常温下蜡烛的两条物理性质:红色固体;不溶于水;密度比水小
(2)点燃蜡烛(图一),能观察到发生化学变化的现象:发光、发热、燃烧等.(写出一条)
(3)取一小木条,迅速平放入火焰中(图二)约一秒后取出,观察到木条表面出现环形焦斑.据此推测,蜡烛火焰中外焰温度最高.
(4)将短玻璃管插入焰心,用燃烧的木条靠近导管另一端(图三),发现导出的气体可以点燃.请你推测导管里气体可能会是石蜡蒸汽.
(5)取一只冷而干燥的小烧杯罩在蜡烛火焰上方(图四),观察烧杯壁上有水珠出现.片刻后取下烧杯,迅速向烧杯中倒入少量澄清的石灰水,振荡,观察到石灰水变浑浊.
据此小明得出蜡烛是由碳、氢元素组成的.你认为他的结论是否正确?不正确.
(6)为了测定蜡烛中碳、氢两 种元素的质量比,小华设计了如图所示的实验.
| 蜡烛 | 装置Ⅱ | 装置Ⅲ | |
| 反应前的质量/g | 15.8 | 182.3 | 212.2 |
| 反应后的质量/g | 14.4 | 184.1 | 216.6 |
先分别称量蜡烛、装置Ⅱ(吸收水)、装置Ⅲ(吸收二氧化碳)的质量.按图示连接好仪器,点燃蜡烛,同时从a导管口抽气.一段时间后熄灭蜡烛,再分别称量蜡烛、装置Ⅱ、装置Ⅲ的质量.
实验数据如上表.请回答:
①该实验中测得水的质量为1.8g.
②由该实验数据计算,蜡烛中碳、氢元素的质量之比为6:1.
③理论上,装置Ⅱ和装置Ⅲ增加的总质量大于蜡烛失去的质量,其原因是与消耗的蜡烛比较,生成的二氧化碳和水中增加了参加反应的氧气所含氧元素质量.
④该实验能否准确测出蜡烛燃烧生成二氧化碳和水的质量?说明理由.
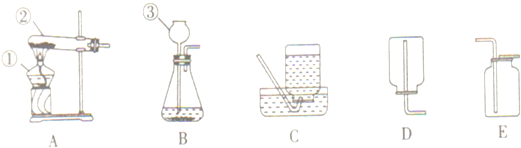
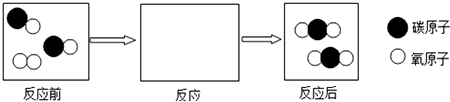
 物质在空气中燃烧,多数只与氧气反应,也有不同的,如镁在空气中燃烧不但与氧气反应,还与氮气和二氧化碳反应.如图是测定空气中燃烧氧气含量的装置图,燃烧匙内放入红磷,测得氧气约占空气总体积的$\frac{1}{5}$.
物质在空气中燃烧,多数只与氧气反应,也有不同的,如镁在空气中燃烧不但与氧气反应,还与氮气和二氧化碳反应.如图是测定空气中燃烧氧气含量的装置图,燃烧匙内放入红磷,测得氧气约占空气总体积的$\frac{1}{5}$.