题目内容
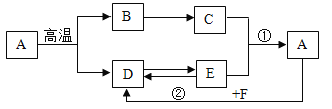
【题目】过氧化钙(CaO2)是用途广泛的优良供氧剂。以电石渣[主要成分为 Ca(OH)2,含少量 CaCO3] 为原料制备 CaO2 的一种工艺流程如图甲所示:
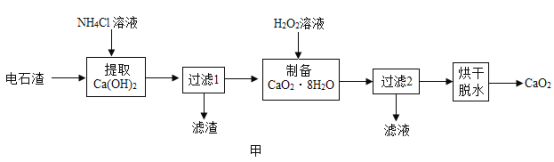
(查阅资料)Ⅰ.Ca(OH)2+2NH4Cl=CaCl2+2NH3H2O
Ⅱ.CaCl2+2NH3H2O+H2O2+6H2O=CaO28H2O↓+2NH4Cl
Ⅲ.CaO28H2O在水中不太稳定,会缓慢分解
(1)CaO2 与 CO2 反应除了生成氧气外、还生成一种常见的盐,写出反应的化学方程式___________。
(2)“提取 Ca(OH)2”时反应的基本类型是__________________;Ca(OH)2 的俗名为___________________;“过滤 1”所得滤渣的主要成分是______________。
(3)在实验室进行过滤操作时,要遵循“一贴、二低、三靠”原则。其中“一贴”指的是滤纸紧贴漏斗壁, 原因是_______________________。实验室粗略测定溶液的酸碱度,常使用(填名称)_________________。
(4)在其他条件不变的情况下,制备 CaO2·8H2O 的反应时间(t)对其产率(ω )的影响如图乙所示。
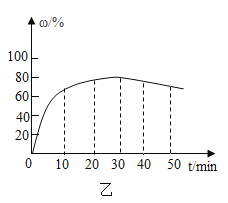
①平均反应速率最快的时间段为___________。
②30min 后,ω 开始下降的主要原因是_________________。
(5)为了测定加入的 NH4Cl 溶液中溶质的质量分数,取 107.0gNH4Cl 溶液于烧杯中,加入稍过量的 AgNO3 溶液,完全反应后过滤、洗涤、干燥、称量, 得到14.35 g 白色固体。通过计算确定该溶液中NH4Cl 的质量分数为________。(精确到 0.1%)
【答案】2CaO2 + 2CO2=2 CaCO3↓+ O2↑ 复分解反应 熟石灰或消石灰 CaCO3 加快过滤速率 pH试纸 0~10min CaO28H2O在水中不太稳定会缓慢分解 5%
【解析】
(1)CaO2 与 CO2 反应除了生成氧气外、还生成一种常见的盐,根据质量守恒定律反应前后元素不变,可推知生成的盐为碳酸钙,反应的化学方程式2CaO2 + 2CO2=2 CaCO3↓+ O2↑;
(2) “提取Ca(OH)2”时氢氧化钙与氯化铵反应生成氯化钙、氨气和水,反应的基本类型是复分解反应;Ca(OH)2的俗名为熟石灰或消石灰;“过滤1”所得滤渣的主要成分是CaCO3;
(3) 在实验室进行过滤操作时,要遵循“一贴、二低、三靠”原则。其中“一贴”指的是滤纸紧贴漏斗内壁, 原因是如果滤纸和漏斗内壁不紧贴会导致过滤太慢。实验室粗略测定溶液的酸碱度,常使用pH试纸;
(4) ①据图可以看出,平均反应速率最快的时间段为0~10min;
②30min后,w开始下降是因为CaO28H2O在水中不太稳定会缓慢分解;
(5)设氯化铵的质量为x

![]()
x=5.35g
故该溶液中NH4Cl的质量分数为:![]()

【题目】下列对客观事实书写的化学方程式及其反应类型都正确的是( )
选项 | 客观事实 | 化学方程式 | 基本反应类型 |
A | 铁丝在氧气中燃烧 | 2Fe+3O2 | 化合反应 |
B | 加热高锰酸钾 | 2KMnO4 | 分解反应 |
C | 乙醇燃烧 | C2H5OH+3O2 | 氧化反应 |
D | 硫酸钾溶液和氯化钡溶液反应 | K2SO4+BaCl2=2KCl +BaSO4 | 复分解反应 |
A.AB.BC.CD.D