题目内容
请你与小明一起进行实验室制取二氧化碳的研究
(1) 选择药品 。小明对三组药品进行了研究,实验记录如下:
|
组别 |
药品 |
实验现象 |
|
① |
块状石灰石和稀盐酸 |
产生气泡速率适中 |
|
② |
块状石灰石和稀硫酸 |
产生气泡速率缓慢并逐渐停止 |
|
③ |
碳酸钠粉末和稀盐酸 |
产生气泡速率很快 |
从制取和收集的角度分析,一般选第①组药品,该组药品发生反应的文字表达式为
;不选择第③组药品的原因是
(2) 选择装置。他认为能选择用过氧化氢制氧气的发生装置。你认为他选择气体发生装置的依据是
(3) 制取气体。将药品装入所选装置制取气体,他认为只能用向上排空气法收集,是因为
(4) 气体检验。将生成的气体通入石蕊中,石蕊变红。原因是(用反应的文字表达式表示) 。由此实验他确定该气体一定是二氧化碳。他的检验方法是否正确?请说明理由
(5) 提供简易装置完成二氧化碳的制取、收集和验满。

上图是实验桌上摆放好的该实验所需用品,小明发现缺少一种实验仪器和一种药品,仪器名称 ;药品名称

(6) 上图是小明实验的主要步骤,这些步骤的正确顺序是 (填字母序号,下同),其中操作有误的是
(7) 如果在实验过程中要向试管中添加酸溶液,要求不改变实验装置,可选用 来完成。
(8) 如果要用上述仪器完成用高锰酸钾制取氧气,还需增加的玻璃仪器是
文字表达式
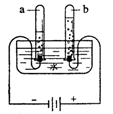
(9) 用如右图所示装置收集二氧化碳,则应该从 端
通入二氧化碳(填字母序号)

①碳酸钙+盐酸 氯化钙+水+二氧化碳; 反应速度太快,生成的气体来不及收集。
氯化钙+水+二氧化碳; 反应速度太快,生成的气体来不及收集。
② 固体和液体在常温(或不加热)反应(或反应物的状态和反应条件)
③二氧化碳密度比空气大且能溶于水。(缺一不可)
④水+二氧化碳 碳酸;
碳酸;
不正确,因为其他气体也能使石蕊变红(或能使石蕊变红的气体不止一种或应该用澄清石灰水检验)。
⑤镊子; 稀盐酸
⑥ cabde ; d
⑦注射器
⑧酒精灯; 高锰酸钾 锰酸钾+二氧化锰+氧气
(9) c
锰酸钾+二氧化锰+氧气
(9) c
【解析】:(1)二氧化碳的制取药品很多,从实验现象中可以看出:三种药品都产生二氧化碳,但是块状石灰石和稀硫酸反应一会儿停止,碳酸钠粉末与稀盐酸反应速度太快,无法收集;因此,选择块状石灰石和稀盐酸来制取二氧化碳.反应原理为CaCO3+2HCl=CaCl2+H2O+CO2↑.
(2)发生装置的选择是根据反应物的状态和反应条件,分固体加热型和固液反应不需加热型两种;
(3)注意“只能”两个字;
(4)能使紫色石蕊变红的气体不一定是二氧化碳,酸性气体都具备这一性质;
(5)取用块状固体用镊子,还缺少液体药品稀盐酸;
(6)制取气体前先检查装置的气密性,最后要洗刷仪器;验满二氧化碳时应把燃着的木条放在集气瓶口,而不能伸入内部;
(7)实验过程中添加溶液,要保证装置不漏气,可以用注射器;
(8)高锰酸钾制取氧气需要加热,所以还需要酒精灯;
(9)由于二氧化碳的密度比空气大,所以应由c端通入。

 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案(1)实验过程:
①把石灰水加入盛有碳酸钠溶液的烧杯中充分搅拌,发生反应的化学方程式:______
②再通过过滤操作,得到无色滤液.
③将无色滤液通过______操作,得到白色固体.
(2)作出猜想:得到的白色固体是纯氢氧化钠吗?三位同学分别作出以下猜想:
小玲:是纯净的氢氧化钠!小明:可能还含有碳酸钠!
小强:也可能含有______.
(3)验证实验:请你来验证小明的猜想.
| 实 验 操 作 | 实验现象 | 实验结论 |
| 取少量白色固体配成溶液,加入足量稀盐酸 | ______ | ______ |
(1)实验过程:
①把石灰水加入盛有碳酸钠溶液的烧杯中充分搅拌,发生反应的化学方程式:______
②再通过过滤操作,得到无色滤液.
③将无色滤液通过______操作,得到白色固体.
(2)作出猜想:得到的白色固体是纯氢氧化钠吗?三位同学分别作出以下猜想:
小玲:是纯净的氢氧化钠!小明:可能还含有碳酸钠!
小强:也可能含有______.
(3)验证实验:请你来验证小明的猜想.
| 实 验 操 作 | 实验现象 | 实验结论 |
| 取少量白色固体配成溶液,加入足量稀盐酸 | ______ | ______ |