题目内容
钠、镁、铝分别与足量稀硫酸反应,生成等质量氢气时,参加反应的钠、镁、铝的原子数目之比是( )A.1:2:3
B.3:2:1
C.6:3:2
D.4:2:1
【答案】分析:先计算出产生等质量的氢气需要三种金属的质量比,再用三种金属的质量除以金属的相对原子质量,算出原子个数比.
解答:解:根据金属的质量× =生成氢气的质量,设钠、镁、铝的质量分别为X、Y、Z则:X×
=生成氢气的质量,设钠、镁、铝的质量分别为X、Y、Z则:X× =Y×
=Y× =Z×
=Z× ,可得X:Y:Z=23:12:9,所以钠、镁、铝的原子数目之比为:
,可得X:Y:Z=23:12:9,所以钠、镁、铝的原子数目之比为: :
: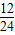 :
: =6:3:2.
=6:3:2.
故选C.
点评:在利用:金属的质量× =生成氢气的质量这一公式时,金属必须能与酸反应,适用于选择题、填空题.
=生成氢气的质量这一公式时,金属必须能与酸反应,适用于选择题、填空题.
解答:解:根据金属的质量×
 =生成氢气的质量,设钠、镁、铝的质量分别为X、Y、Z则:X×
=生成氢气的质量,设钠、镁、铝的质量分别为X、Y、Z则:X× =Y×
=Y× =Z×
=Z× ,可得X:Y:Z=23:12:9,所以钠、镁、铝的原子数目之比为:
,可得X:Y:Z=23:12:9,所以钠、镁、铝的原子数目之比为: :
: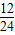 :
: =6:3:2.
=6:3:2.故选C.
点评:在利用:金属的质量×
 =生成氢气的质量这一公式时,金属必须能与酸反应,适用于选择题、填空题.
=生成氢气的质量这一公式时,金属必须能与酸反应,适用于选择题、填空题. 
练习册系列答案
相关题目
钠、镁、铝分别与足量稀硫酸反应,生成等质量氢气时,参加反应的钠、镁、铝的原子数目之比是( )
| A、1:2:3 | B、3:2:1 | C、6:3:2 | D、4:2:1 |