题目内容
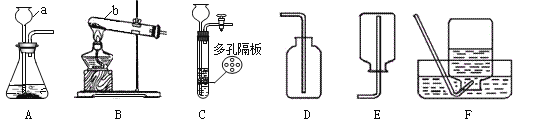
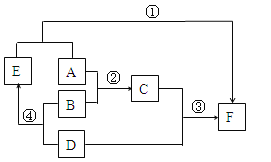
【题目】(14分)某校兴趣小组同学准备进行常见酸、碱、盐的性质实验时,发现实验台上摆放的药品中(如下图),有一瓶溶液的试剂瓶未盖瓶盖且标签破损,于是决定对这瓶溶液进行实验探究:
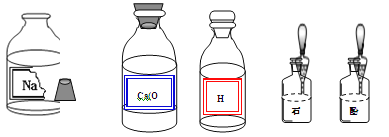
【提出问题】这瓶溶液是什么溶液?
【获得信息】酸、碱、盐的性质实验中用到含有钠元素的物质是氯化钠、氢氧化钠、碳酸钠
【提出猜想】这瓶溶液是:猜想一:氯化钠溶液;猜想二:氢氧化钠溶液;猜想三:碳酸钠溶液。
【实验推断】(1)小丽取样滴加无酚酞试液,溶液呈红色,得出结论:该溶液不可能是 溶液。
(2)小刚另取样滴加稀盐酸有 产生,小刚得出结论:该溶液是碳酸钠溶液。
(3)小青认为小刚的结论不完全正确,理由 。
小组同学讨论后一致认为还需要进行如下实验:
【继续探究】另取样加入过量的CaCl2溶液,观察到有 产生,设计这一步骤的目的是 ;静置后,取上层清液,滴入酚酞试液,溶液呈红色。
【实验结论】这瓶溶液是 。
【探究启示】实验取完药品后应 。
【答案】(1)氯化钠 (2)气体 (3)氢氧化钠变质后生成的碳酸钠也会和盐酸反应生成气体。
【继续探究】白色沉淀 除尽溶液中的碳酸钠
【结论】氢氧化钠溶液
【实验启示】密封保存
【解析】
试题分析:
【实验推断】
(1)取样滴加无酚酞试液,溶液呈红色,说明溶液呈碱性,由于氯化钠呈中性,故不可能是氯化钠;
(2)滴加稀盐酸,若是碳酸钠,碳酸钠会与盐酸反应生成二氧化碳气体,现象是产生大量的气泡;
(3)根据题意,该试剂瓶未盖瓶盖,那么该试剂可能是氢氧化钠,原因是氢氧化钠易与空气中二氧化碳反应生成碳酸钠而发生了变质;
【继续探究】
另取样加入过量的CaCl2溶液,氯化钙会与碳酸钠反应生成氯化钠和碳酸钙沉淀,由于氯化钙是过量的,故能把碳酸钠完全除去;静置后,取上层清液,滴入酚酞试液,溶液呈红色,说明反应后的溶液呈碱性,由于氯化钙和生成的氯化钠均是呈中性,故说明溶液中含有另一种呈碱性的物质,即是氢氧化钠,从而这么这瓶溶液是氢氧化钠溶液,溶液中的碳酸钠是由于氢氧化钠与空气中的二氧化碳反应生成的,由此也知,我们实验完毕后要及时盖上瓶塞,防止溶液变质。

 智慧小复习系列答案
智慧小复习系列答案【题目】(6分)化学是在原子、分子水平上研究物质及其变化的科学。
(1)现有下列化学式或粒子符号:①2CO ②Ca2+ ③2H ④O2。其中,“2”表示两个分子的是 (填序号,下同),表示每个粒子带两个单位电荷的是_______;
(2)一定条件下,甲和乙反应生成丙和丁(四种物质均由分子构成),反应前后微观示意图如图所示。下列说法正确的是 (填字母编号)。
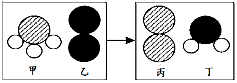
A.反应前后共有4种原子
B.该反应有单质生成
C.反应前后元素化合价都不变
D.化学变化中分子和原子均可再分
E.该化学反应中,甲、丁两种分子的个数比是2:3
(3)胃酸过多须服用抗酸药。下表为两种抗酸药的有效成分及其构成粒子:
抗胃酸药 | 复方氢氧化镁片剂 | 铝碳酸镁片 |
有效成分 | Mg(OH)2 | AlMg(OH)3CO3 |
构成粒子 | Mg2+、OH- | Al3+、Mg2+、OH-、CO32- |
由于抗酸药有效成分不同,起抗酸作用(即消耗胃液中盐酸)的粒子也有差异。
①Mg(OH)2起抗酸作用的粒子是 (填粒子符号,下同);
②铝碳酸镁与盐酸的反应为:AlMg(OH)3CO3 + 5HCl == MgCl2 + AlCl3 + 4H2O + CO2↑。
铝碳酸镁起抗酸作用的两种粒子是 、 。