题目内容
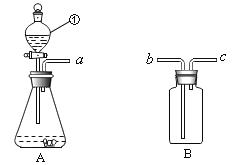
【题目】【2016年江苏省宿迁市】 某兴趣小组同学欲探究NaOH溶液与CO2气体的反应,设计如图所示实验装置:
(1)若导管a与b连接,将分液漏斗中的NaOH溶液注入锥形瓶,关闭分液漏斗上的活塞,振荡,然后打开导管上的活塞,观察到的实验现象是________,CO2与NaOH反应的化学方程式是________;
(2)探究反应后锥形瓶内溶液中溶质的成分:
已知Na2CO3+H2O+CO2═2NaHCO3 NaHCO3+NaOH═Na2CO3+H2O
【提出猜想】Ⅰ.NaOH和Na2CO3;Ⅱ.________;
Ⅲ.NaHCO3; Ⅳ.Na2CO3和NaHCO3.
【查阅资料】①Ca(OH)2与Na2CO3、NaHCO3均能反应且有白色沉淀生成;
②CaCl2与Na2CO3能反应且有白色沉淀生成,与NaHCO3不反应;
③NaHCO3溶液显碱性,可与酸反应生成CO2气体。
【设计实验】限选试剂:Ca(OH)2溶液、CaCl2溶液、稀盐酸、酚酞试液.
实验操作 | 实验现象 | 实验结论 |
1.取少量反应后溶液于试管中,加入足量的________振荡 | 产生白色沉淀 _________ | 猜想Ⅲ不成立 |
2.将操作Ⅰ所得混合物过滤,向滤液中加入足量的_________,振荡 | _________ | 猜想Ⅳ成立 |
【拓展应用】联想到空气中有CO2,所以实验室中的氢氧化钠溶液应_________保存。

【答案】(1)烧杯内的水流入锥形瓶中,2NaOH+CO2═Na2CO3+H2O;
(2)【提出猜想】Na2CO3;
【设计实验】
实验操作 | 实验现象 | 实验结论 |
1.氯化钙 | 产生白色沉淀 | |
2.稀盐酸 | 有气泡产生 |
【拓展应用】密封。
【解析】(1)二氧化碳和氢氧化钠反应后气压会减小,烧杯内的水流入锥形瓶中,CO2与NaOH反应生成碳酸钠和水,化学方程式为:2NaOH+CO2═Na2CO3+H2O;(2)【提出猜想】二氧化碳和氢氧化钠反应时,如果氢氧化钠过量,则溶质是氢氧化钠和碳酸钠;如果二氧化碳过量,但是不能完全消耗生成的碳酸钠,则溶质是碳酸钠和碳酸氢钠;如果氢氧化钠和二氧化碳恰好完全反应,则溶质是碳酸钠;如果二氧化碳过量,并且把碳酸钠完全消耗,则溶质是碳酸氢钠,所以猜想II是Na2CO3;因二氧化碳不但能跟氢氧化钠反应,二氧化碳还能溶于水也跟水反应.所以让人产生质疑;
【设计实验】
实验操作 | 实验现象 | 实验结论 |
1.取少量反应后溶液于试管中,加入足量的氯化钙振荡 | 产生白色沉淀 | 猜想Ⅲ不成立 |
2.将操作Ⅰ所得混合物过滤,向滤液中加入足量的稀盐酸,振荡 | 有气泡产生 | 猜想Ⅳ成立 |
【拓展应用】空气中的二氧化碳会与氢氧化钠反应,所以实验室中的氢氧化钠溶液应密封保存。

 高效智能课时作业系列答案
高效智能课时作业系列答案 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案