题目内容
分类归纳是学习化学的重要方法.①H
2+CuO
Cu+H
2O ②C+2CuO
2Cu+CO
2↑ ③CO+CuO
Cu+CO
2是初中阶段学到的三个重要反应.其中的每个反应既存在氧化反应又存在还原反应,可称为氧化还原反应.反应中表现出氧化性的物质称之为氧化剂,表现出还原性的物质称之为还原剂.
(1)三个反应中的氧化剂是
.制得相同质量的铜,反应掉的还原剂质量最少的是
(填序号).
(2)分析以上反应你会发现,还原剂中一定存在化合价
(填“升高”或“降低”、“不变”)的元素.
(3)根据你的发现,判断反应Cl
2+2NaBr=2NaCl+Br
2中的还原剂是
.
分析:氧化剂提供氧,化合价降低,具有氧化性,发生还原反应;还原剂得到氧,化合价升高,具有还原性,发生氧化反应.
解答:解:(1)从三个反应①H
2+CuO
Cu+H
2O ②C+2CuO
2Cu+CO
2↑ ③CO+CuO
Cu+CO
2,可知氧化铜失去氧,是氧化剂,氢气、炭、一氧化碳都得到氧,作还原剂;当制得相同质量的同时,反应的还原剂质量最小的是氢气;
(2)分析以上反应,还原剂氢气中氢元素的化合价由0价升高到+1价,碳单质中碳元素化合价由0价升高到+4价,一氧化碳中碳元素的化合价由+2升高到+4价,都存在化合价升高的元素;
(3)根据以上分析,可知还原剂存在化合价升高的元素,NaBr中溴的化合价由-1价升高到0价,化合价升高,是还原剂.
故答案为:
(1)CuO,①;(2)升高;(3)NaBr.
点评:要熟记和理解碳、一氧化碳、氢气还原氧化铜实验的化学反应方程式、装置、操作及注意事项和现象,以及金属铜的冶炼原理、氧化还原反应,结合所学的相关知识和技能,细致地阅读、分析题意,细心地进行探究、推理,最后,按照题目的要求,认真地进行解答即可.
 一题一题找答案解析太慢了
一题一题找答案解析太慢了
下载作业精灵直接查看整书答案解析立即下载
练习册系列答案
相关题目


 Cu+H2O ②C+2CuO
Cu+H2O ②C+2CuO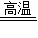 2Cu+CO2↑ ③CO+CuO
2Cu+CO2↑ ③CO+CuO Cu+CO2是初中阶段学到的三个重要反应.其中的每个反应既存在氧化反应又存在还原反应,可称为氧化还原反应.反应中表现出氧化性的物质称之为氧化剂,表现出还原性的物质称之为还原剂.
Cu+CO2是初中阶段学到的三个重要反应.其中的每个反应既存在氧化反应又存在还原反应,可称为氧化还原反应.反应中表现出氧化性的物质称之为氧化剂,表现出还原性的物质称之为还原剂.