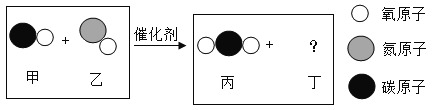
题目内容
【题目】写出下列反应的化学方程式,并在括号里注明反应的基本类型:
(1)过氧化氢与二氧化锰混合制氧气_________________,_______反应;
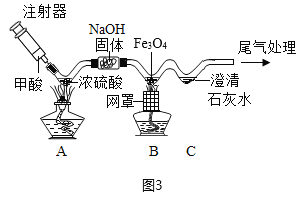
(2)铁丝在氧气中燃烧__________________,_______反应;
(3)铜丝浸入硝酸银溶液中__________________,_______反应;
(4)镁在二氧化碳中燃烧生成氧化镁和炭黑__________________。
【答案】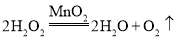 分解反应
分解反应 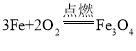 化合反应
化合反应 ![]() 置换反应
置换反应 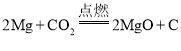
【解析】
(1)过氧化氢和二氧化锰作用生成水和氧气,化学方程式为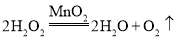 ,该反应符合“一变多”特点属于分解反应,故填:
,该反应符合“一变多”特点属于分解反应,故填: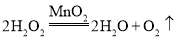 ;分解反应。
;分解反应。
(2)铁丝在氧气中燃烧生成四氧化三铁,化学方程式为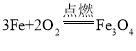 ,该反应符合“多变一”特点,属于化合反应,故填:
,该反应符合“多变一”特点,属于化合反应,故填: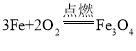 ;化合反应。
;化合反应。
(3)铜丝浸入硝酸银溶液中和硝酸银反应生成硝酸铜和银,化学方程式为![]() ,该反应反应物是单质和化合物,生成物是单质和化合物,符合置换反应特点,属于置换反应,故填:
,该反应反应物是单质和化合物,生成物是单质和化合物,符合置换反应特点,属于置换反应,故填:![]() ;置换反应。
;置换反应。
(4)镁在二氧化碳中燃烧生成氧化镁和炭黑化学方程式为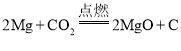 ,故填:
,故填: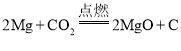 。
。

【题目】化学实验小组的同学们对催化剂产生了兴趣,通过查阅资料了解到氧化铁也能加速氯酸钾的分解。为了探究氧化铁能否加快过氧化氢的分解,他们设计了实验装置,并进行气体的制备和测量实验。实验时均以生成40mL气体为标准,相关实验数据记录如下表:
实验序号 | 过氧化氢溶液浓度/% | 过氧化氢溶液体积/mL | 过氧化氢溶液温度/℃ | 氧化铁的用量/g | 收集40mL氧气所需时间/s |
① | 5 | 10 | 20 | 0 | 128.5 |
② | 5 | 10 | 20 | 1.2 | 16.8 |
③ | 15 | 10 | 20 | 1.2 | 10.5 |
④ | 5 | 10 | 70 | 0 | 32.7 |
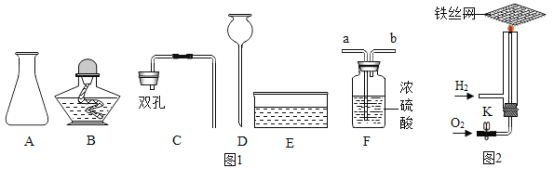
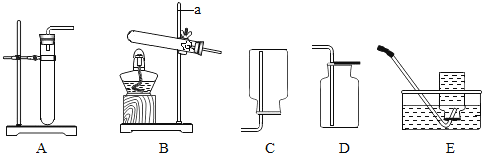
(1)完成上述实验及数据的测定需要用到下图中的部分装置,请按组装顺序写出所用到的装置代号____。
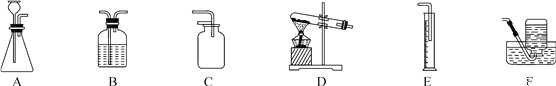
(2)通过实验①和④对比可知,化学反应速率与温度的关系是_______;通过实验②和③对比可知,化学反应速率与______有关;通过实验_______和______对比可知,氧化铁可以加快过氧化氢分解放氧的速率。
(3)若要证明氧化铁是过氧化氢分解的催化剂,还需要验证它在该反应前后的___和____未发生改变。
(4)同学们还想探究催化剂的颗粒大小对化学反应速率是否有影响,请你帮他们设计实验方案进行探究:_______。