题目内容
【题目】金属用途十分广泛,牢固掌握金属的知识很有必要。
(1)下列关于金属的说法中不正确的是_____(填字母序号)
A 大多数金属都是银白色的 B 铁是地壳中含量最高的金属 C 金的活动性比较弱 D 水银在常温下是液体
(2)“曾青得铁则化为铜”是炼铜的原理,请用化学方程式表示其原理。_____。
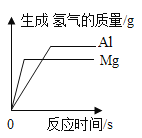
(3)铝在金属活动性顺序中位于氢前面,可小林发现铝与稀盐酸开始反应时铝表面几乎没有气泡产生。请分析产生该现象的原因。_____。
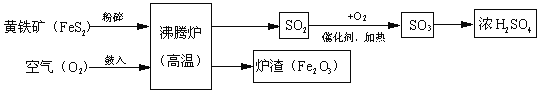
(4)为了研究炼铁原理,在老师的指导下,同学们在实验室的通风橱内利用如图所示装置(其他实验用品略),进行一氧化碳与氧化铁反应的实验,请你一起参与。


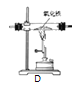
①实验室制得的一氧化碳中常混有二氧化碳和水蒸气,欲用纯净、干燥的一氧化碳还原氧化铁并检验生成的气体,上述装置的正确连接顺序是制得的CO→_____(填装置序号,装置不得重复使用)。
②装置A的作用是_____。
③装置D的玻璃管内发生反应的化学方程式为_____。
④该实验产生的尾气会造成环境污染,请你提出处理尾气的方法_____。
(5)铜的金属活动性虽然位于氢之后,但资料中显示铜可以和稀硝酸反应,其化学方程式为3Cu+8HNO3=3Cu(NO3)2+4H2O+2M,则M的化学式为_____。现将1.92g铜加到50g稀硝酸中,巧好完全反应,求稀硝酸中溶质的质量分数_____。
【答案】B Fe+CuSO4=FeSO4+Cu 铝性质很活泼,很容易和空气中的氧气反应生成一层致密的氧化膜,导致和盐酸接触是生成水而不生成氢气 B→A→D→C 除去一氧化碳中混有的水蒸气 Fe2O3+3CO![]() 2Fe+3CO2 点燃或者收集 NO 10.08%。
2Fe+3CO2 点燃或者收集 NO 10.08%。
【解析】
(1)根据金属性质和特性分析;
(2)根据“曾青得铁则化为铜”的化学本质书写化学方程式。
(3)根据铝氧化后的特点分析;
(4)根据实验目的确定仪器连接顺序;
(5)根据铜的质量和对应的化学方程式求算稀硝酸中溶质的质量分数。
(1)
A.大多数金属都是银白色的。正确,不符合题意;
B.铝是是地壳中含量最高的金属。错误,符合题意;
C.金的活动性比较弱。正确,不符合题意;
D.水银在常温下是液体,正确,不符合题意;
故选:B。
(2)“曾青得铁则化为铜”是铁和可溶性铜盐反应生成亚铁盐和铜,对应化学方程式可以为 Fe+CuSO4=FeSO4+Cu。
(3)铝性质很活泼,很容易和空气中的氧气反应生成一层致密的氧化膜,导致铝和盐酸接触开始是氧化铝与稀盐酸反应生成水和氯化铝,而不生成氢气。
(4)
①实验室制得的一氧化碳中常混有二氧化碳和水蒸气,欲用纯净、干燥的一氧化碳还原氧化铁并检验生成的气体,由于给出的要求为“装置不得重复使用”即理解为每一步进行很彻底,所以先净化、后干燥,然后反应并检验,正确连接顺序是制得的CO→B→A→D→C。
②装置A的作用是除去一氧化碳中混有的水蒸气。
③装置D的玻璃管内发生反应是一氧化碳和氧化铁在高温下生成铁和二氧化碳,对应的化学方程式为 Fe2O3+3CO![]() 2Fe+3CO2。
2Fe+3CO2。
④该实验产生的尾气可能混有一氧化碳,而一氧化碳有毒,所以可以点燃或者收集。
(5)根据3Cu+8HNO3=3Cu(NO3)2+4H2O+2M,可知反应前:Cu原子3个,H原子 8个,N 原子8个,O原子24个;而反应后现有:Cu原子3个,H原子 8个,N原子 6个,O原子22个;缺少 N 原子2个,O原子2个,分布在2个M分子中,所以每个分子含有一个氮原子和一个氧原子,M的化学式为 NO。
设稀硝酸中溶质的质量分数为x。
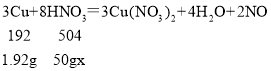
![]()
x=10.08%

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】呼吸面具中“氧气再生剂”的主要成分是淡黄色固体过氧化钠(Na2O2),使用后变成白色固体.某兴趣小组对白色固体的成分进行探究:
(查阅资料)2Na2O2+2CO2=2Na2CO3+O2;2Na2O2+2H2O=2NaOH+O2↑
(1)(提出猜想)根据呼出的气体中含有较多的_____.对白色固体作出如下猜想:
猜想Ⅰ:氢氧化钠猜想Ⅱ:碳酸钠猜想Ⅲ:氢氧化钠和碳酸钠
(2)(实验验证)
实验操作 | 实验现象 | 实验结论 |
(1)取少量样品溶于水,加入足量_____; | 产生白色沉淀; | 该反应的化学方程式为_____; |
(2)将上述反应后的混合物过滤,取滤液加入_____. | _____. | 证明猜想Ⅲ正确. |
(3)(得出结论)猜想Ⅲ成立.
(拓展应用)“氧气再生剂”的保存方法是_____.