题目内容
人类对原子结构的认识永无止境.
(1)道尔顿认为原子是“不可再分的实心球体”,汤姆生认为原子是“嵌着葡萄干的面包”,如今这些观点均______(填“正确”或“错误”),卢瑟福进行α粒子散射实验后,认为原子是“行星模型”,即原子是由带______电荷的原子核和核外电子构成.
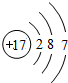
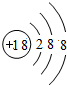
(2)上图是元素周期表的一部分(数字表示相应元素的原子序数).表中部分元素的原子(离子)结构示意图如下,其中属于阳离子的是______(填数字序号).
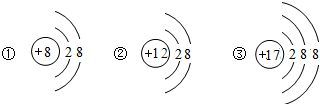
选用表中元素填空A2B2型化合物的化学式是______,带一个单位负电荷的一种阴离子______.某耐火材料是由Mg,O组成的化合物,写出其化学式______.

(1)道尔顿认为原子是“不可再分的实心球体”,汤姆生认为原子是“嵌着葡萄干的面包”,如今这些观点均______(填“正确”或“错误”),卢瑟福进行α粒子散射实验后,认为原子是“行星模型”,即原子是由带______电荷的原子核和核外电子构成.
| 1H | |||||||
| 8O | |||||||
| 12Mg | 17Cl | ||||||

选用表中元素填空A2B2型化合物的化学式是______,带一个单位负电荷的一种阴离子______.某耐火材料是由Mg,O组成的化合物,写出其化学式______.

(1)原子是由居于原子中心的带正电的原子核和核外电子构成,而非“嵌着葡萄干的面包”或“不可再分的实心球体”;
故答案为:错误;正(或+);
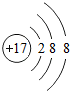
(2)微粒①③均为质子数小于核外电子数的阴离子,微粒②为质子数大于核外电子数的阳离子;
H、Mg、O、Cl四种元素中,H、Mg元素呈正价,O、Cl易得电子而呈负价,其中能形成H、O元素可形成H2O2;
氯原子最外层7个电子,易得1个电子而形成带一个单位负电荷的Cl-,氢氧根离子OH-也为带一个负电荷的阴离子;
镁原子最外层2个电子,易失2个电子,氧原子最外层6个电子,易得2个电子,因此,两元素化合时形成化合物的化学式为MgO;
故答案为:②;H2O2;Cl-(或OH-);MgO.
故答案为:错误;正(或+);
(2)微粒①③均为质子数小于核外电子数的阴离子,微粒②为质子数大于核外电子数的阳离子;
H、Mg、O、Cl四种元素中,H、Mg元素呈正价,O、Cl易得电子而呈负价,其中能形成H、O元素可形成H2O2;
氯原子最外层7个电子,易得1个电子而形成带一个单位负电荷的Cl-,氢氧根离子OH-也为带一个负电荷的阴离子;
镁原子最外层2个电子,易失2个电子,氧原子最外层6个电子,易得2个电子,因此,两元素化合时形成化合物的化学式为MgO;
故答案为:②;H2O2;Cl-(或OH-);MgO.

练习册系列答案
 一卷搞定系列答案
一卷搞定系列答案 名校作业本系列答案
名校作业本系列答案 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案
相关题目
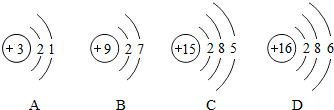
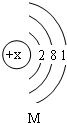

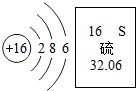
 ,则该粒子是( )
,则该粒子是( )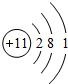
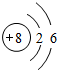
 下列有关说法正确的是( )
下列有关说法正确的是( )