题目内容
【题目】科学探究和证据推理是化学学科的核心素养。某小组对碱式碳酸铜晶体[Cu2(OH)2CO3]的性质进行实验探究,并基于证据进行推理分析。
(1)分析碱式碳酸铜的组成
根据化学式可知,碱式碳酸铜中Cu元素的化合价为___________价。
(2)探究碱式碳酸铜受热的变化
[设计实验]该小组设计了如图装置(夹持仪器已略去),并用于探究碱式碳酸铜的分解产物。
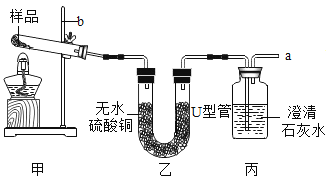
[实验过程]
①在装置丙导管a处连接一导管,并插入水中,微热试管,观察到______________,说明整套装置的气密性良好。
②按图示加入样品和试剂,加热一段时间后, 试管中固体变黑,U形管中无水硫酸铜变蓝,澄清石灰水变浑浊。
[实验分析]
注:无水硫酸铜为白色固体,遇水变蓝。
①装置甲中加热时先____________,后对准药品部位集中加热。
②装置丙中发生反应的化学方程式为____________。
③根据现象可知,碱式碳酸铜受热可分解,分解产物有CO2、CuO、____________。
④装置乙、丙位置不能互换的理由是____________。
【答案】+2 导管口出现气泡 预热 ![]() H2O 气体通过澄清石灰水时会带出水蒸气,无法检验是否生成水
H2O 气体通过澄清石灰水时会带出水蒸气,无法检验是否生成水
【解析】
二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水;碱式碳酸铜能与硫酸发生反应,生成硫酸铜、水和二氧化碳。
(1)碱式碳酸铜的化学式为Cu2(OH)2CO3,氧元素的化合价为-2价,碳元素的化合价为+4价,氢元素的化合价为+1价,设铜元素的化合价为x,化合物中各元素化合价代数和为零,![]() ,
,![]() ,故碱式碳酸铜中Cu元素的化合价为+2价。
,故碱式碳酸铜中Cu元素的化合价为+2价。
(2)①在装置丙导管a处连接一导管,并插入水中,微热试管,试管中的空气受热膨胀,从短管口逸出,故观察到导管口出现气泡,说明整套装置的气密性良好。
[实验分析]
①为防止受热不均匀使试管炸裂,故给装置甲中加热时先预热,后对准药品部位集中加热。
②装置丙中发生反应是二氧化碳和氢氧化钙生成碳酸钙和水,反应的化学方程式为
![]() 。
。
③U形管中无水硫酸铜变蓝,说明反应生成水,澄清石灰水变浑浊,说明反应生成二氧化碳,碱式碳酸铜受热可分解,分解产物有CO2、CuO、H2O。
④石灰水中有水,装置乙、丙位置不能互换的理由是气体通过澄清石灰水时会带出水蒸气,无法检验是否生成水。

 特高级教师点拨系列答案
特高级教师点拨系列答案【题目】图表法是一种常用的数据处理方法,根据所给图表(氢氧化钠、碳酸钠分别在水、酒精中的溶解度如表所示),下列说法正确的是( )
氢氧化钠 | 碳酸钠 | |||
20℃ | 40℃ | 20℃ | 40℃ | |
水 | 109g | 129g | 21.8g | 49g |
酒精 | 17.3g | 40g | 不溶 | 不溶 |

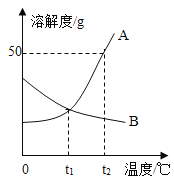
A. 上述图象表示碳酸钠的溶解度曲线
B. 20℃时,氢氧化钠的溶解度大于碳酸钠
C. 40℃时,若将 50g NaOH 分别投入到 100g 水和 100g 酒精中,都能形成饱和溶液
D. 40℃时,将适量 CO2 通入饱和的 NaOH 酒精溶液中,观察不到明显的现象