题目内容
汽车是现代生活中不可缺少的代步工具.请回答下列问题:
(1)汽车电路中的导线多数是用铜制做的,这是利用了金属铜的导电性和________性.
(2)下列汽车配件及用品中,用合金制做的是(填字母)________.a.钢铁外壳b.玻璃车窗c.橡胶轮胎d.真皮座椅
(3)铁在潮湿的空气中容易锈蚀.
①汽车表面喷漆,可以延缓汽车的锈蚀,其防锈原理是隔绝空气(氧气)和________.
②喷漆前需将铁制品放入稀盐酸中除锈(铁锈主要成分是Fe2O3),反应初期可观察到溶液由无色变为黄色,这是因为生成了________(填化学式);反应进行一会儿,又可以观察到有无色气泡产生,该反应的化学方程式是________.
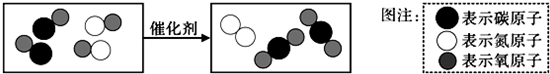
(4)“尾气催化转化器”可将汽车尾气中的有毒气体转化为无毒气体,图表示治理汽车尾气所涉及反应的微观过程. 图中所示反应的化学方程式为________;
解:(1)铜具有导电性,能用作导线,铜具有延展性,能被拉成铜丝,故填:延展;
(2)a钢属于合金,b玻璃属于无机硅酸盐材料,c橡胶属于有机高分子材料,d真皮属于天然材料,故填:a;
(3)①铁在有水和氧气并存时易生锈,在铁制品表面刷漆能隔绝氧气和水,故填:水;
②氧化铁与盐酸反应生成的氯化铁的水溶液呈黄色,铁能与盐酸反应生成氯化亚铁和氢气,故填:FeCl3; Fe+2HCl=FeCl2+H2↑;
(4)据图可知,此反应是一氧化碳与一氧化氮在催化剂的作用下生成了氮气和二氧化碳,故填:2CO+2NO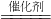 N2+2CO2.
N2+2CO2.
分析:根据物质的性质进行分析,金属具有导电性和延展性,根据物质的类别即可判断,盐酸能与金属氧化物以及活泼金属发生化学反应,根据微观粒子的分子构成即可写出有关反应的化学方程式.
点评:本题考查了金属的性质以及有关反应方程式的书写,完成此题,可以依据题干提供的信息结合物质的性质进行.
(2)a钢属于合金,b玻璃属于无机硅酸盐材料,c橡胶属于有机高分子材料,d真皮属于天然材料,故填:a;
(3)①铁在有水和氧气并存时易生锈,在铁制品表面刷漆能隔绝氧气和水,故填:水;
②氧化铁与盐酸反应生成的氯化铁的水溶液呈黄色,铁能与盐酸反应生成氯化亚铁和氢气,故填:FeCl3; Fe+2HCl=FeCl2+H2↑;
(4)据图可知,此反应是一氧化碳与一氧化氮在催化剂的作用下生成了氮气和二氧化碳,故填:2CO+2NO
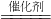 N2+2CO2.
N2+2CO2.分析:根据物质的性质进行分析,金属具有导电性和延展性,根据物质的类别即可判断,盐酸能与金属氧化物以及活泼金属发生化学反应,根据微观粒子的分子构成即可写出有关反应的化学方程式.
点评:本题考查了金属的性质以及有关反应方程式的书写,完成此题,可以依据题干提供的信息结合物质的性质进行.

练习册系列答案
相关题目



