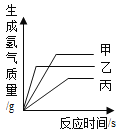
题目内容
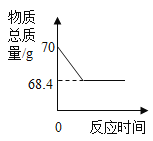
【题目】草木灰是农家肥料,它的主要成分是碳酸钾。某化学兴趣小组取100g草木灰于烧杯中,不断滴入稀盐酸溶液,当滴入40g稀盐酸时,不再有气泡产生,此时烧杯中的残余混合物质量为137.8g。碳酸钾与盐酸反应的化学方程式为K2CO3+2HCl=2KC1+H2O+CO2↑(假设草木灰的其他成分不与盐酸反应),请计算回答:
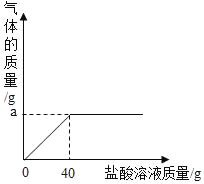
(1)如图表示反应过程放出的气体质量与加入盐酸的关系曲线,请根据质量守恒定律求出图中纵坐标上a点数值:a=______g
(2)草木灰样品中碳酸钾的质量分数______(要求写出计算过程)。
【答案】2.2 6.9%
【解析】
解:(1)质量守恒定律可知,图中纵坐标上a点数值表示为生成二氧化碳的质量,二氧化碳的质量为100g+40g﹣137.8g=2.2g;
(2)设碳酸钾的质量为x,
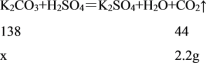
![]()
x=6.9g
草木灰样品中碳酸钾的质量分数=![]() ×100%=6.9%
×100%=6.9%
答:草木灰样品中碳酸钾的质量分数为6.9%。

【题目】蔗糖是生活中常见的一种物质,某兴趣小组对“蔗糖的组成”进行了探究。
(做出猜想)小组同学认为绿色植物通过光合作用将二氧化碳和水转化成葡萄糖和氧气葡萄糖进一步转化为蔗糖,故蔗糖中一定含有碳、氢元素,可能含有氧元素。
(实验验证)
方案一:小明将蔗糖在氧气中燃烧,检验到生成物中有水和二氧化碳,得出结论“蔗糖是由碳、氢、氧三种元素组成的”,小刚认为该方案不合理,只能说明蔗糖中一定含有碳、氢元素,不能确定是否含有氧元素,理由是______。
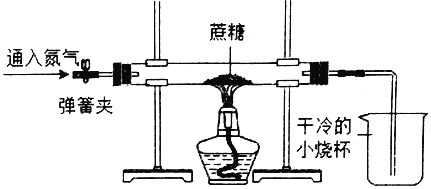
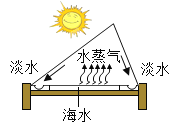
方案二:小刚用如图所示的装置进行实验。实验开始先通入一会儿氮气,然后关闭弹簧夹,点燃酒精灯给蔗糖加强热。
![]() 观察到______,说明蔗糖中含有氢元素和氧元素。
观察到______,说明蔗糖中含有氢元素和氧元素。
![]() 观察到硬质玻璃管中残留有黑色固体,他猜测该黑色固体是单质碳,并继续利用如图所示装置,另选试剂进行了验证单质碳的实验。实验过程和现象如表:
观察到硬质玻璃管中残留有黑色固体,他猜测该黑色固体是单质碳,并继续利用如图所示装置,另选试剂进行了验证单质碳的实验。实验过程和现象如表:
实验操作 | 实验现象 |
往硬质玻璃管中通入 ______ , 并在小烧杯中加入 ______ ,点燃酒精灯 | ①硬质玻璃管中的黑色固体剧烈燃烧,发出白光; ②______ |
![]() 写出上述实验过程中一个反应的化学方程式:______。
写出上述实验过程中一个反应的化学方程式:______。
(实验结论)蔗糖是由碳、氢、氧三种元素组成的。
(拓展交流)方案二中,先通入一会儿氮气的原因是______。
【题目】某同学为测定黄铜屑(由锌和铜形成的合金)样品组.分四次取样品与稀盐酸反应,其实验数据记录见下表.
1 | 2 | 3 | 4 | |
取样品质量(g) | 50.0 | 50.0 | 50.0 | 50.0 |
取稀硫酸质量(g) | 40.0 | 80.0 | 120.0 | 160.0 |
产生气体质量(g) | 0.4 | 0.8 | 1.0 | 1.0 |
试计算:
①第几次实验金属锌完全反应______.
②所用稀硫酸中溶质的质量分数_______?