题目内容
(5分)碳酸钡广泛应用于显像管(CRT)、陶瓷、光学玻璃等行业。现有碳酸盐矿石(主要成分是BaCO3和CaCO3),以下是从该矿石中分离出BaCO3的流程图。(已知:钡元素化合物的化学性质与钙元素化合物的化学性质相近。)
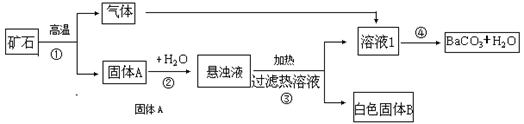
试回答下列问题:
(1) 已知不同温度下Ca(OH)2和Ba(OH)2的溶解度如下表:
步骤③加热悬浊液,过滤热溶液的原因是 ;
(2)现在25℃时,将10g氢氧化钡放入50g水中,充分搅拌,所得溶液的溶质质量分数为 。(精确到0.1%)
(3)步骤①中产生的气体是 ;步骤④中发生化学反应的方程式为
。
(4)绿色化学又称环境友好化学,其核心是利用化学原理来减少和消除工业生产对环境的影响。上述流程中体现绿色化学理念的是:
。

试回答下列问题:
(1) 已知不同温度下Ca(OH)2和Ba(OH)2的溶解度如下表:
| 温度(℃) | 0 | 20 | 25 | 60 |
| Ba(OH)2溶解度 | 1.67 | 3.89 | 5.60 | 20.94 |
| Ca(OH)2溶解度 | 0.189 | 0.173 | 0.148 | 0.121 |
(2)现在25℃时,将10g氢氧化钡放入50g水中,充分搅拌,所得溶液的溶质质量分数为 。(精确到0.1%)
(3)步骤①中产生的气体是 ;步骤④中发生化学反应的方程式为
。
(4)绿色化学又称环境友好化学,其核心是利用化学原理来减少和消除工业生产对环境的影响。上述流程中体现绿色化学理念的是:
。
(1)原因是 温度越高氢氧化钡的溶解度越大,氢氧化钙的溶解度越小,因此在较高温度下过滤得到的氢氧化钡溶液中所含氢氧化钙杂质就越少 ;
(2) 5.3% 。(精确到0.1%)
(3)气体是 CO2;
化学方程式 CO2+Ba(OH)2=" BaCO3" ↓+ H2O 。
(4) 步骤①中产生的二氧化碳气体在步骤④中得到充分的利用,减少排放
(2) 5.3% 。(精确到0.1%)
(3)气体是 CO2;
化学方程式 CO2+Ba(OH)2=" BaCO3" ↓+ H2O 。
(4) 步骤①中产生的二氧化碳气体在步骤④中得到充分的利用,减少排放
(1)对比所给出的氢氧化钙、氢氧化钡的溶解度表,会得到随温度升高氢氧化钙溶解度降低而氢氧化钡溶解度升高;温度越高氢氧化钡的溶解度越大,氢氧化钙的溶解度越小,因此在较高温度下过滤得到的氢氧化钡溶液中所含氢氧化钙杂质就越少;
(2)25℃时氢氧化钡的溶解度为5.60g,此时将10g氢氧化钡放入50g水中,充分搅拌,所得溶液为饱和溶液,其溶质的质量分数="5.60g" /(100g+5.60g)×100%=5.3%;
(3)根据钡元素化合物的化学性质与钙元素化合物的化学性质相近的信息,可知矿石A高温下发生分解所产生的气体为二氧化碳;分解所得二氧化碳通入过滤所得氢氧化钡溶液即溶液1中,二氧化碳与氢氧化钡反应生成碳酸钡沉淀和水,化学方程式为CO2+Ba(OH)2=BaCO3↓+H2O;
(4)根据绿色化学的核心是利用化学原理来减少和消除工业生产对环境的影响,而流程中反应④消耗分解时所产生的二氧化碳,可减少向大气中的排放量,有效保护环境,体现出绿色化学的理念
(2)25℃时氢氧化钡的溶解度为5.60g,此时将10g氢氧化钡放入50g水中,充分搅拌,所得溶液为饱和溶液,其溶质的质量分数="5.60g" /(100g+5.60g)×100%=5.3%;
(3)根据钡元素化合物的化学性质与钙元素化合物的化学性质相近的信息,可知矿石A高温下发生分解所产生的气体为二氧化碳;分解所得二氧化碳通入过滤所得氢氧化钡溶液即溶液1中,二氧化碳与氢氧化钡反应生成碳酸钡沉淀和水,化学方程式为CO2+Ba(OH)2=BaCO3↓+H2O;
(4)根据绿色化学的核心是利用化学原理来减少和消除工业生产对环境的影响,而流程中反应④消耗分解时所产生的二氧化碳,可减少向大气中的排放量,有效保护环境,体现出绿色化学的理念

练习册系列答案
相关题目
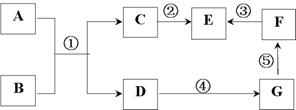
 ="=" NH3↑+HCl↑
="=" NH3↑+HCl↑