题目内容
【题目】溶液在生产、生活和实验中起着十分重要的作用。请回答下列问题:
(1)某同学配制100g溶质质量分数为5%的氯化钠溶液,请回答下列问题:
①若用氯化钠固体和水配制,实验步骤为计算、______ 、量取、溶解。
②若用溶质质量分数为20%的氯化钠溶液和水配置,则需20%的氯化钠溶液质量为____g。
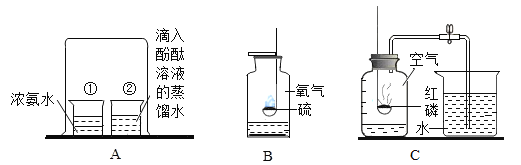
(2)向装有等量水的A、B、C烧杯中分别加入10g、25g、25gNaNO3固体,充分溶解后,现象如图一所示。

①图一烧杯中的溶液一定属于饱和溶液的是_______(填序号);要使NaNO3不饱和溶液变为饱和可以采取的方法是___________。
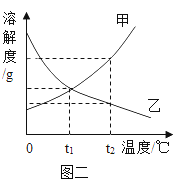
②图二能表示NaNO3溶解度曲线的是_________(填“甲”或“乙”);甲、乙两物质溶解度曲线的交点的含义是______。
【答案】称量 25 B 增加溶质(或降低温度或蒸发溶剂) 甲 t1℃时甲乙两种物质的溶解度相同
【解析】
(1)①配制100g溶质质量分数为5%的氯化钠溶液,首先计算配制溶液所需氯化钠和水的质量,再称量所需的氯化钠和量取水,最后进行溶解,故正确配制该溶液的操作顺序为计算、称量、量取、溶解。故填:称量。
②用溶质质量分数为20%的氯化钠溶液来配制该溶液,设需要需20%的氯化钠溶液的质量为x,则20%x=100g×5%,x=25g。故填:25。
(2)①向装有等量水的A、B、C烧杯中分别加入10g、25g、25gNaNO3固体,充分溶解后,由于在三个烧杯中只有B有未溶解的固体存在,因此B中的溶液一定是饱和溶液。A、C烧杯中没有未溶解的固体存在,不能确定能否再溶解硝酸钠,所以不能确定是否是不饱和溶液。由图一B、C可知,NaNO3的溶解度随温度的升高而增大,所以让NaNO3的不饱和溶液变为饱和溶液,可以采取:降低温度、蒸发溶剂、加溶质;故填:B;增加溶质(或降低温度或蒸发溶剂)。
②由题意可知,在等量的30℃的水中全部溶解了25g硝酸钠,而20℃的水没有全部溶解25g硝酸钠,说明硝酸钠的溶解度随温度的升高而增大。故能表示NaNO3溶解度曲线的是甲;t1℃时,甲、乙两物质的溶解度曲线相交于一点,二者的溶解度相同;故填:甲;t1℃时甲乙两种物质的溶解度相同。

 名校课堂系列答案
名校课堂系列答案