题目内容
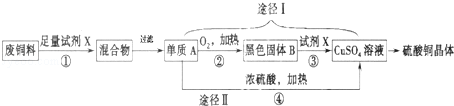
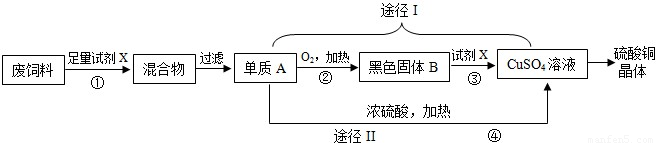
硫酸铜溶液常用于农业上制波尔多液.如图是用废铜料(铁、铜混合物)来生产硫酸铜的过程,请根据图示回答下列问题.

(1)反应①的基本类型为 ;
(2)③反应的化学方程式为 ;
(3)已知:Cu+2H2SO4(浓)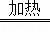 CuSO4+SO2↑+2M.则M的化学式为 ;对比途径I、Ⅱ,途径I的优点有: .
CuSO4+SO2↑+2M.则M的化学式为 ;对比途径I、Ⅱ,途径I的优点有: .
【解析】
试题分析:废铜料中有铁和铜,要生产硫酸铜,需将铁除去,因此可加入足量稀硫酸将铁除去,铜与硫酸不反应,过滤后铜与氧气反应转化为氧化铜,氧化铜和硫酸反应生成硫酸铜。
(1)反应①为铁与硫酸反应生成硫酸亚铁和氢气,化学方程式为Fe+H2SO4 ═FeSO4+H2↑反应物是一种单质和一种化合物,生成物是另一种单质和另一种化合物,属于置换反应.
(2)反应③是氧化铜与硫酸反应生成硫酸铜和水,化学方程式为CuO+H2SO4═CuSO4+H2O
(3)根据反应前后原子种类和数目不变可知,反应前氢原子4个,氧原子8个,铜原子1个,硫原子2个,反应后已有铜原子1个,硫原子2个,氧原子6个,因此2M中含有4个氢原子和2个氧原子,故M的化学式为H2O;途径Ⅰ转化的化学方程式为2Cu+O2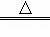 2CuO,CuO+H2SO4═CuSO4+H2O;途径Ⅱ是铜与浓硫酸反应生成硫酸铜、二氧化硫和水,因此对比途径I、Ⅱ,途径Ⅰ没有二氧化硫产生,无污染
2CuO,CuO+H2SO4═CuSO4+H2O;途径Ⅱ是铜与浓硫酸反应生成硫酸铜、二氧化硫和水,因此对比途径I、Ⅱ,途径Ⅰ没有二氧化硫产生,无污染

练习册系列答案
相关题目

 CuSO4+SO2↑+2M.则M的化学式为
;对比途径I、Ⅱ,途径I的优点有:
.
CuSO4+SO2↑+2M.则M的化学式为
;对比途径I、Ⅱ,途径I的优点有:
.
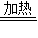 CuSO4+SO2↑+2M.则M的化学式为 ;对比途径I、Ⅱ,途径I的优点有: .
CuSO4+SO2↑+2M.则M的化学式为 ;对比途径I、Ⅱ,途径I的优点有: .