题目内容
【题目】推理是常用的学习方法。下列推理正确的是
A.酸的水溶液显酸性,所以显酸性的溶液一定是酸溶液
B.氯化钠和硫酸铜都含有金属离子,属于盐,则所有盐中都含有金属离子
C.活泼金属能与盐酸反应产生气体,所以能与盐酸反应产生气体的物质一定是活泼金属
D.由一种元素组成的纯净物一定是单质,则单质一定只含一种元素
【答案】D
【解析】
A、酸的水溶液显酸性,但是显酸性的溶液不一定是酸溶液,可能是盐溶液,故错误;
B、铵盐中不含有金属离子,故错误;
C、能与盐酸反应产生气体的物质可能是金属,也可能是碳酸盐,故错误;
D、由一种元素组成的纯净物一定是单质,则单质一定只含一种元素,正确。故选D。

【题目】某化学兴趣小组利用以下装置探究气体的制取及性质。结合下图回答有关问题: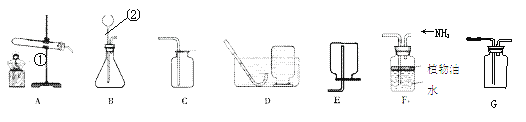
(1)图中标号的仪器名称① , ②。
(2)若选择氯酸钾制取氧气,该反应的化学方程式为 若用装置G收集氧气,氧气应从 端通入(选填“左”或“右”)。
(3)已知NH3极易溶于水且能与水反应,密度比空气小,实验室可用固体氢氧化钙[Ca(OH)2]和固体氯化铵(NH4Cl)加热来制取NH3 , 同时生成氯化钙(CaCl2)和水, 则可选用的发生和收集装置组合是 , 若用F装置收集NH3 , 油层的作用是 。
(4)小华通过互联网得知:多种物质都能催化过氧化氢的分解。【初次探究】实验证明,在过氧化氢溶液中滴加CuSO4溶液能显著加快过氧化氢的分解,如果要确定CuSO4是催化剂,还必须通过实验确定它在化学反应前后质量和不变
【再次探究】CuSO4溶液主要含有三种粒子(H2O、Cu2+、SO42-),稀硫酸中含有三种粒子(H2O、H+、SO42-)为了进一步探究CuSO4溶液中哪种粒子能起催化作用。小华作了以下分析和设计。
①小华认为最不可能的是H2O,他的理由是 。
②要说明另外的两种粒子是否起到催化作用,小华设计了如下实验,完成探究活动。
实验步骤 | 实验现象 | 实验结论 |
a. 取一支试管加入5mL5%过氧化氢溶液,然后加入2-3滴稀硫酸 | 溶液几乎没有气泡放出 | 实验证明,起催化作用的是 |
b. 另取一支试管加入5mL5%过氧化氢溶液,然后加入2-3滴氯化铜溶液 | 溶液中有大量气泡放出 |