题目内容
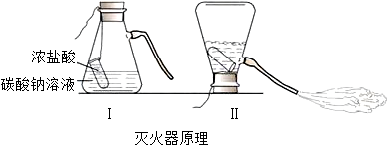 (2012?保山)某兴趣小组在学习“灭火器原理”后,设计了如图所示实验,对反应后锥形瓶中残留液体进行了探究.
(2012?保山)某兴趣小组在学习“灭火器原理”后,设计了如图所示实验,对反应后锥形瓶中残留液体进行了探究.提出问题:废液中所含的溶质是什么?
猜想与假设:
猜想Ⅰ:废液中的溶质是NaCl和HCl.
猜想Ⅱ:废液中的溶质是NaCl和Na2CO3.
猜想Ⅲ:废液中的溶质只有(1)
NaCl
NaCl
.实验与探究:
(2)为验证猜想Ⅱ成立,可选用
稀盐酸
稀盐酸
试剂,观察到的实验现象是:有气泡产生
有气泡产生
.(3)为验证猜想Ⅰ成立,小勇同学取少量废液于试管中,滴加AgNO3溶液,产生白色沉淀,再加稀硝酸沉淀不溶解.于是小勇认为猜想Ⅰ正确,请你对小勇得出的结论进行评价,
不正确,因为NaCl和HCl都能跟AgNO3溶液产生白色沉淀
不正确,因为NaCl和HCl都能跟AgNO3溶液产生白色沉淀
.(4)CO2能灭火利用了其
不能燃烧也不支持燃烧
不能燃烧也不支持燃烧
的化学性质.分析:猜想与假设:(1)根据发生的反应,废液的可能组成是:①恰好完全反应,废液中的溶质只有氯化钠,②浓盐酸有剩余,废液中含有氯化钠和氯化氢,③碳酸钠有剩余,废液中含有碳酸钠和氯化钠.
实验与探究:(2)根据碳酸钠能与稀酸反应生成二氧化碳分析解答即可;
(3)根据氯化钠也能与硝酸银反应生成氯化银的白色沉淀分析解答;
(4)依据二氧化碳的化学性质分析解答;
实验与探究:(2)根据碳酸钠能与稀酸反应生成二氧化碳分析解答即可;
(3)根据氯化钠也能与硝酸银反应生成氯化银的白色沉淀分析解答;
(4)依据二氧化碳的化学性质分析解答;
解答:解:猜想与假设:(1)根据碳酸钠与盐酸反应可以生成氯化钠,所以废液的可能组成是:①恰好完全反应,废液中的溶质只有氯化钠,②浓盐酸有剩余,废液中含有氯化钠和氯化氢,③碳酸钠有剩余,废液中含有碳酸钠和氯化钠.
实验与探究:(2)因为碳酸钠能与稀酸反应生成二氧化碳,所以加入试剂如果反应时出现了气泡,则说明溶质中含有碳酸钠,则猜想II成立;
(3)由于盐酸、氯化钠都能与硝酸银反应生成氯化银的白色沉淀(不溶于硝酸),所以不能确定猜想(1)正确;
(4)二氧化碳能灭火是因为二氧化碳具有不能燃烧也不支持燃烧的化学性质;
故答案为:(1)NaCl(2)稀盐酸; 有气泡产生;(3)不正确,因为也能跟AgNO3溶液产生白色沉淀;(4)不能燃烧也不支持燃烧;
实验与探究:(2)因为碳酸钠能与稀酸反应生成二氧化碳,所以加入试剂如果反应时出现了气泡,则说明溶质中含有碳酸钠,则猜想II成立;
(3)由于盐酸、氯化钠都能与硝酸银反应生成氯化银的白色沉淀(不溶于硝酸),所以不能确定猜想(1)正确;
(4)二氧化碳能灭火是因为二氧化碳具有不能燃烧也不支持燃烧的化学性质;
故答案为:(1)NaCl(2)稀盐酸; 有气泡产生;(3)不正确,因为也能跟AgNO3溶液产生白色沉淀;(4)不能燃烧也不支持燃烧;
点评:本题考查了碳酸钠与盐酸的反应以及碳酸钠和氯离子的检验,完成此题,可以依据碳酸钠和盐酸的性质以及常见离子的检验方法进行.

练习册系列答案
 智能训练练测考系列答案
智能训练练测考系列答案
相关题目