题目内容
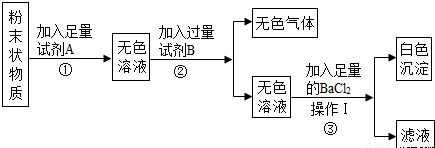
(2011?兰州)实验室有一包粉末状物质,可能由NaCl、Na2SO4、Na2CO3、FeCl3中的一种或几种组成.为了确定原粉末的成分,某校化学兴趣小组的同学,按下图所示进行实验:

请回答下列问题:(填化学式)
(1)若A是相对分子质量最小的氧化物,则A为
(2)该粉末中一定不含
(3)为了不干扰对第③步实验现象的判断,试剂B最好选择

请回答下列问题:(填化学式)
(1)若A是相对分子质量最小的氧化物,则A为
H2O
H2O
;无色气体是CO2
CO2
.(2)该粉末中一定不含
FeCl3
FeCl3
,操作Ⅰ的名称是过滤
过滤
.(3)为了不干扰对第③步实验现象的判断,试剂B最好选择
稀盐酸
稀盐酸
,请写出步骤③的化学方程式:Na2SO4+BaCl2═2NaCl+BaSO4↓
Na2SO4+BaCl2═2NaCl+BaSO4↓
.分析:根据(1)中A为相对分子质量最小的氧化物是水,加水后得到是无色溶液,氯化铁的水溶液为黄色,可以确定没有氯化铁,能够生成气体的物质只有碳酸钠,即试剂B为盐酸,而无色气体为二氧化碳,由于加入的盐酸是过量的,所以得到的白色沉淀为硫酸钡,即在原混合物中含有硫酸钠,操作I为过滤.至此分析完毕,可以据此答题.
解答:解:(1)A为相对分子质量最小的氧化物可以知道A为水,加入过量B后得到无色气体,在这里能够生成气体的只有碳酸钠,所以可以判断含有碳酸钠,那么生成的无色气体为二氧化碳.
(2)加入试剂B后得到是无色溶液,由于氯化铁溶液呈黄色,所以可以推断该粉末中不含氯化铁,对于操作I后得到是固体也滤液,所以可以判断操作I为过滤.
(3)根据所加的试剂氯化钡可以判断出生成的白色沉淀为硫酸钡,所以为了防止对实验结果的干扰,试剂B最好加入的是盐酸,故步骤③是硫酸钠和氯化钡的反应.
故答案为:(1)H2O; CO2
(2)FeCl3;过滤
(3)稀盐酸; Na2SO4+BaCl2═2NaCl+BaSO4↓
(2)加入试剂B后得到是无色溶液,由于氯化铁溶液呈黄色,所以可以推断该粉末中不含氯化铁,对于操作I后得到是固体也滤液,所以可以判断操作I为过滤.
(3)根据所加的试剂氯化钡可以判断出生成的白色沉淀为硫酸钡,所以为了防止对实验结果的干扰,试剂B最好加入的是盐酸,故步骤③是硫酸钠和氯化钡的反应.
故答案为:(1)H2O; CO2
(2)FeCl3;过滤
(3)稀盐酸; Na2SO4+BaCl2═2NaCl+BaSO4↓
点评:本题为文字叙述型物质推断题,完成此题,要抓住语言叙述的关键,根据给出的物质之间的反应,找准解题突破口,做出判断.熟记化学方程式:Na2SO4+BaCl2═2NaCl+BaSO4↓.

练习册系列答案
相关题目
(2011?兰州)同学们在实验室发现了三种金属--铝、铁、铜,其中一块铜片生锈了,表面附有部分铜绿[铜绿的主要成分是Cu2(OH)2CO3],他们的实验探究过程如下:
(1)铜绿是铜与空气中的氧气、水和(填化学式)共同作用的结果.
(2)为探究铝、铁、铜的活动性顺序,某同学设计了一组实验:①铝片浸入稀硫酸中;②铜片浸入稀硫酸中;③铝片浸入氯化亚铁溶液中,这组实验还不能完全证明三种金属的活动性顺序.请你补充一个实验来达到实验目的(写出实验步骤、现象).
(3)他们还想用加热的方法除去铜绿,加热时却发现铜片表面全部变黑.经查阅资料知道:①铜绿受热分解会生成黑色的氧化铜 ②酒精在不完全燃烧时会生成炭黑 ③炭黑与稀硫酸不以应.
a、他们提出猜想:该黑色物质可能是氧化铜,也可能是氧化铜和的混合物.
b、设计了下述实验方案,用于检验黑色物质.
(1)铜绿是铜与空气中的氧气、水和(填化学式)共同作用的结果.
(2)为探究铝、铁、铜的活动性顺序,某同学设计了一组实验:①铝片浸入稀硫酸中;②铜片浸入稀硫酸中;③铝片浸入氯化亚铁溶液中,这组实验还不能完全证明三种金属的活动性顺序.请你补充一个实验来达到实验目的(写出实验步骤、现象).
(3)他们还想用加热的方法除去铜绿,加热时却发现铜片表面全部变黑.经查阅资料知道:①铜绿受热分解会生成黑色的氧化铜 ②酒精在不完全燃烧时会生成炭黑 ③炭黑与稀硫酸不以应.
a、他们提出猜想:该黑色物质可能是氧化铜,也可能是氧化铜和的混合物.
b、设计了下述实验方案,用于检验黑色物质.
| 实验步骤 | 实验现象 | 结论 |
| 剪下一片变黑的铜片,放入盛有足量稀硫酸的试管中,微热 | 铜片表面黑色固体全部消失,露出红色的铜,溶液变色. | 此黑色固体是(填化学式) |