题目内容
有一包白色固体粉末可能由NH4NO3,Na2CO3、BaCl2、CuSO4、NaCl中的一种或几种组成.为了确定其组成,小东做了以下实验:
①取少量白色粉末于研钵中,加入少量的熟石灰粉末混合,研磨,没有闻到氨味;
②另取少量白色粉末加入到适量的水中,出现白色浑浊,静置后,上层清液无色;
③小心倒掉上层清液,向沉淀中加入稀硝酸,白色沉淀完全溶解,并有无色无味的气体产生.
由以上实验可推断:
(1)这包白色固体中肯定存在 ,肯定不存在 ;
(2)写出②中出现白色浑浊的化学方程式 .
①取少量白色粉末于研钵中,加入少量的熟石灰粉末混合,研磨,没有闻到氨味;
②另取少量白色粉末加入到适量的水中,出现白色浑浊,静置后,上层清液无色;
③小心倒掉上层清液,向沉淀中加入稀硝酸,白色沉淀完全溶解,并有无色无味的气体产生.
由以上实验可推断:
(1)这包白色固体中肯定存在
(2)写出②中出现白色浑浊的化学方程式
考点:物质的鉴别、推断,盐的化学性质,书写化学方程式、文字表达式、电离方程式
专题:混合物组成的推断题
分析:根据题中所给的物质都溶于水,硫酸铜在溶液中显蓝色,碳酸根离子和钡离子会生成碳酸钡沉淀,硫酸根离子和钡离子会生成硫酸钡沉淀,碳酸钡会溶于酸生成二氧化碳,铵态氮肥在碱性环境中会生成有刺激性气味的氨气进行分析.
解答:解:题中所给的物质都溶于水,硫酸铜在溶液中显蓝色,碳酸根离子和钡离子会生成碳酸钡沉淀,硫酸根离子和钡离子会生成硫酸钡沉淀,碳酸钡会溶于酸生成二氧化碳,铵态氮肥在碱性环境中会生成有刺激性气味的氨气.
取少量白色粉末于研钵中,加入少量的熟石灰粉末混合,研磨,没有闻到氨味,说明白色粉末中一定没有硝酸铵,另取少量白色粉末加入到适量的水中,出现白色浑浊,静置后,上层清液无色,因此白色粉末中一定没有硫酸铜,白色沉淀可能是碳酸钡,也可能是硫酸钡,小心倒掉上层清液,向沉淀中加入稀硝酸,白色沉淀完全溶解,并有无色无味的气体产生,那么白色沉淀一定是碳酸钡,因此混合物中一定有Na2CO3和BaCl2,白色粉末中是否含有氯化钠不会影响题中的实验现象,所以这包白色固体中肯定存在Na2CO3和BaCl2,肯定不存在CuSO4和NH4NO3.
故答案为:Na2CO3和BaCl2,CuSO4和NH4NO3.
取少量白色粉末于研钵中,加入少量的熟石灰粉末混合,研磨,没有闻到氨味,说明白色粉末中一定没有硝酸铵,另取少量白色粉末加入到适量的水中,出现白色浑浊,静置后,上层清液无色,因此白色粉末中一定没有硫酸铜,白色沉淀可能是碳酸钡,也可能是硫酸钡,小心倒掉上层清液,向沉淀中加入稀硝酸,白色沉淀完全溶解,并有无色无味的气体产生,那么白色沉淀一定是碳酸钡,因此混合物中一定有Na2CO3和BaCl2,白色粉末中是否含有氯化钠不会影响题中的实验现象,所以这包白色固体中肯定存在Na2CO3和BaCl2,肯定不存在CuSO4和NH4NO3.
故答案为:Na2CO3和BaCl2,CuSO4和NH4NO3.
点评:在解此类题时,首先分析所给混合物中各物质的性质,然后根据题中所给的实验现象进行判断各种物质的存在性,最后确定混合物的组成成分.

练习册系列答案
 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案
相关题目
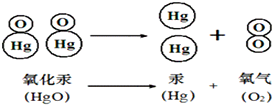 氧化汞受热时的变化可用如图表示,图中大圆圈表示汞原子,小圆圈表示氧原子,据图得出的结论中不正确的是( )
氧化汞受热时的变化可用如图表示,图中大圆圈表示汞原子,小圆圈表示氧原子,据图得出的结论中不正确的是( )| A、所有物质均是由分子构成的 |
| B、分子在化学变化中可以再分 |
| C、原子是化学变化中的最小粒子 |
| D、氧化汞受热时分解生成汞和氧气 |
化学变化的主要特征是( )
| A、颜色、状态发生变化 |
| B、有新的物质生成 |
| C、有气体放出 |
| D、发光、发热、有时有沉淀生成 |
下列关于相对原子质量的说法不正确的是( )
| A、相对原子质量单位为1 |
| B、相对原子质量是一个比值 |
| C、相对原子质量就是原子的实际质量 |
| D、相对原子质量代表各类原子实际质量的相对大小 |
如表列出了20℃时NaNO3溶解实验的一组数据,下列叙述不正确的是( )
| 实验序号 | 水的质量/g | 所加NaCl的质量/g | 所得溶液的质量/g |
| ① | 5 | 3 | 8 |
| ② | 5 | 4 | 9 |
| ③ | 5 | 5 | 9.4 |
| ④ | 5 | 6 | 9.4 |
| A、③所得溶液的溶质质量分数为50% |
| B、①②所得溶液是20℃时NaNO3的不饱和溶液 |
| C、③④所得溶液是20℃时NaNO3的饱和溶液 |
| D、20℃时NaNO3的溶解度为88g |