题目内容
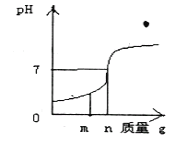
【题目】用熟石灰中和一定量的盐酸,溶液的pH与加入的熟石灰质量的关系如图所示。当加入熟石灰mg时,溶液中的溶质为____;若改用ng氢氧化钠与相同量盐酸反应,所得溶液的pH____7(填“>”“<”或“=”);所得溶液的溶质是____。
【答案】HCl、CaCl2 < NaCl、HCl
【解析】
试题分析:熟石灰与盐酸反应的化学方程式为:Ca(OH)2 +2HCl =CaCl2 + 2H2O;当加入熟石灰mg时,根据图示:溶液的PH小于7,说明盐酸过量,故此时溶液中的溶质为:HCl、CaCl2 ;当加入熟石灰ng时,溶液的PH=7,说明两者恰好完全反应,若改用ng氢氧化钠与相同量盐酸反应,要判断此时溶液的PH,抓住酸碱中和反应的实质:H++OH-=H2O,故只要比较ng熟石灰与ng氢氧化钠中所含的OH-的量,ng×2×17/74×100% >ng×17/40×100%,说明改用ng氢氧化钠,OH-的量减少了,则酸就过量,所以所得溶液的pH<7,所得溶液的溶质是NaCl、HCl

练习册系列答案
 优等生题库系列答案
优等生题库系列答案 53天天练系列答案
53天天练系列答案
相关题目