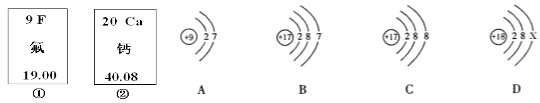
题目内容
【题目】某兴趣小组为测定一瓶过氧化氢溶液中过氧化氢的质量,实验测得相关数据如图所示,请回答下列问题:
①反应生成氧气的质量为g.
②计算该过氧化氢溶液中过氧化氢的质量为g.
【答案】1.6g;3.4g
【解析】解:(1)根据质量守恒定律,反应生成氧气的质量=68g+1.0g-67.4g=1.6g;故填:1.6;(2)设68.0 g过氧化氢溶液中含有过氧化氢的质量为x.
2H2O2 | O2↑ |
68 | 32 |
x | 1.6g |
![]() x=3.4g 过氧化氢溶液的溶质的质量分数=
x=3.4g 过氧化氢溶液的溶质的质量分数= ![]() 。 答:该过氧化氢溶液的溶质的质量分数5.0%。
。 答:该过氧化氢溶液的溶质的质量分数5.0%。
故答案为:1.6g;3.4g;
(2)设68.0 g过氧化氢溶液中含有过氧化氢的质量为x.
2H2O2 | O2↑ |
68 | 32 |
x | 1.6g |
68 x = 32 1.6 g x=3.4g 过氧化氢溶液的溶质的质量分数= 3.4 g 68.0 g × 100 % = 5.0 %
答:该过氧化氢溶液的溶质的质量分数5.0%。
本题主要考察质量守恒定律和依据化学方程式的计算。即反应物质量总和等于新生成物质质量总和;在化学反应中,各物质质量之比等于相对分子质量乘以化学计量数之比。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目