题目内容
某化学研究小组的同学欲对某种塑料袋的组成成分进行分析探究,并测算元素的质量分数,设计了如图所示的实验装置.(资料显示该塑料袋只含碳、氢两种元素,燃烧产物为二氧化碳和水.)图中碱石灰可以吸收空气中的二氧化碳与水蒸气.
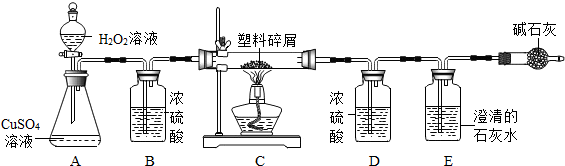
(1)实验时,打开分液漏斗的活塞,将H2O2溶液滴入到A装置的 (填仪器名称)中,再点燃C处的酒精灯,使反应进行.
(2)A装置中CuSO4溶液的作用是 .
(3)通过观察到 的现象,可以判断塑料袋式样中含有碳元素.
(4)根据实验前后D装置的质量变化测算出该塑料袋试样中氢元素的质量分数为14.3%.若装置中没有连接仪器B,则测算出来的氢元素的质量分数会 .(填“偏大”、“偏小”或“不变”)

(1)实验时,打开分液漏斗的活塞,将H2O2溶液滴入到A装置的
(2)A装置中CuSO4溶液的作用是
(3)通过观察到
(4)根据实验前后D装置的质量变化测算出该塑料袋试样中氢元素的质量分数为14.3%.若装置中没有连接仪器B,则测算出来的氢元素的质量分数会
考点:实验探究物质的组成成分以及含量,常见气体的检验与除杂方法,实验室制取氧气的反应原理,质量守恒定律及其应用
专题:科学探究
分析:白色污染是人们对难降解的塑料垃圾(多指塑料袋)污染环境现象的一种形象称谓.它是指用聚苯乙烯、聚丙烯、聚氯乙烯等高分子化合物制成的各类生活塑料制品使用后被弃置成为固体废物,由于随意乱丢乱扔,难于降解处理,以致造成城市环境严重污染的现象;资料显示该种塑料袋只含碳、氢两种元素,燃烧产物为二氧化碳和水.图中碱石灰可以吸收空气中的二氧化碳与水蒸气.则可推测答案.
解答:解:因为白色污染是各类生活塑料制品使用后被弃置成为固体废物,由于随意乱丢乱扔,难于降解处理,以致造成城市环境严重污染的现象,故我国禁止生产、销售、使用超薄塑料购物袋,并实行塑料购物袋有偿使用制度.这样做的主要目的是防止白色污染;资料显示该种塑料袋只含碳、氢两种元素,燃烧产物为二氧化碳和水.图中碱石灰可以吸收空气中的二氧化碳与水蒸气.
(1)实验时,打开分液漏斗的活塞,将H2O2溶液滴入到A装置的锥形瓶中,再点燃C处的酒精灯,使反应进行.
(2)A装置中CuSO4溶液的作用是加快过氧化氢溶液的分解速率.
(3)氢氧化钙与二氧化碳反应,化学方程式为:CO2+Ca(OH)2═CaCO3↓+H2O,故:通过观察到E装置中澄清石灰水变浑浊的现象,可以判断塑料袋式样中含有碳元素.
(4)因为B装置的浓硫酸具有吸水作用,则水会进入D装置会引起质量偏大,所以根据实验前后D装置的质量变化测算出;该塑料袋试样中氢元素的质量分数为14.3%.若装置中没有连接仪器B,则测算出来的氢元素的质量分数会偏大.
故答为:
(1)锥形瓶;
(2)加快过氧化氢溶液的分解速率;
(3)E装置中澄清石灰水变浑浊;
(4)偏大.
(1)实验时,打开分液漏斗的活塞,将H2O2溶液滴入到A装置的锥形瓶中,再点燃C处的酒精灯,使反应进行.
(2)A装置中CuSO4溶液的作用是加快过氧化氢溶液的分解速率.
(3)氢氧化钙与二氧化碳反应,化学方程式为:CO2+Ca(OH)2═CaCO3↓+H2O,故:通过观察到E装置中澄清石灰水变浑浊的现象,可以判断塑料袋式样中含有碳元素.
(4)因为B装置的浓硫酸具有吸水作用,则水会进入D装置会引起质量偏大,所以根据实验前后D装置的质量变化测算出;该塑料袋试样中氢元素的质量分数为14.3%.若装置中没有连接仪器B,则测算出来的氢元素的质量分数会偏大.
故答为:
(1)锥形瓶;
(2)加快过氧化氢溶液的分解速率;
(3)E装置中澄清石灰水变浑浊;
(4)偏大.
点评:本题主要考查学生对白色污染的概念和防止措施的掌握,由此可加强学生的环保意识.

练习册系列答案
相关题目
下列各组变化中均属于化学变化的一组是( )
| A、铁生锈,水结冰,钢锭抽成丝 |
| B、蜡烛熔化,镁燃烧,玻璃破碎 |
| C、碳燃烧,车胎放炮,木材造船 |
| D、煤燃烧,石灰水变浑,石灰石煅烧生石灰 |
物质的性质决定物质的用途,以下用途利用其化学性质的是( )
| A、用石墨做铅笔芯 |
| B、镁粉用做烟火和照明弹 |
| C、干冰用于人工降雨 |
| D、铜丝用做电线 |
澳大利亚科学家发现了纯碳新材料“碳纳米泡沫”,每个泡沫含有约4 000个碳原子,直径约6到9nm,在低于-183℃时,泡沫具有永久磁性.下列叙述正确的是( )
| A、“碳纳米泡沫”是碳单质 |
| B、“碳纳米泡沫”是混合物 |
| C、“碳纳米泡沫”是一种新型的碳化合物 |
| D、“碳纳米泡沫”和金刚石的物理性质完全相同 |
 ”和“
”和“ ”分别表示两种不同的原子,如图所示是构成某些气体粒子的示意图,根据其组成特点回答(填序号)下列问题:
”分别表示两种不同的原子,如图所示是构成某些气体粒子的示意图,根据其组成特点回答(填序号)下列问题: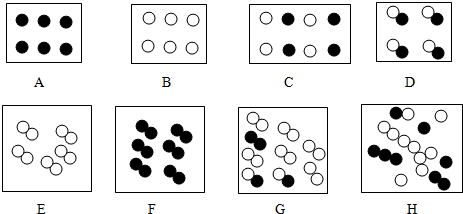
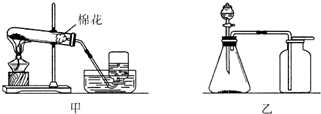 如图是实验室制取氧气的两种装置,请回答下列问题.
如图是实验室制取氧气的两种装置,请回答下列问题.