题目内容
【题目】用下图所示装置分离CO和CO2 的混合气体,回答下列问题(提示:实验所用试剂均为足量):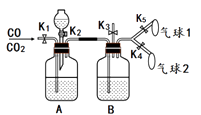
(1)试剂瓶B中盛有浓硫酸,其作用是。在气球1中首先收集到的气体是。
(2)整个实验过程A中发生反应的化学方程式为。
(3)要收集较纯净的二氧化碳应进行的操作(装置中各开关处于关闭状态)是。
【答案】
(1)干燥,CO
(2)2NaOH + CO2 = Na2CO3 + H2O,Na2CO3+H2SO4 =Na2SO4+H2O+CO2↑
(3)打开K3,将分液漏斗中稀硫酸放入广口瓶中,将燃着的木条放在管口,木条熄灭,关闭K3,打开K4
【解析】根据实验目的和要求可知,试剂瓶A中盛放的是氢氧化钠溶液,B中盛放的是浓硫酸(1)试剂瓶B中盛有浓硫酸,起到干燥气体的作用;在气球1中首先收集到的气体是一氧化碳,因为二氧化碳被试剂瓶A中的氢氧化钠溶液吸收;(2)整个过程中实验过程A中首先发生反应的化学方程式为2NaOH + CO2 = Na2CO3 + H2O;然后滴加硫酸使之与碳酸钠反应生成二氧化碳,方程式为Na2CO3+H2SO4 =Na2SO4+H2O+CO2↑;(3)要收集较纯净的二氧化碳应进行的操作(装置中各开关处于关闭状态)是打开K3 ,将分液漏斗中稀硫酸放入广口瓶中,将燃着的木条放在管口,木条熄灭,关闭K3,打开K4。
所以答案是:(1)干燥;一氧化碳(CO);(2)2NaOH + CO2 = Na2CO3 + H2O;Na2CO3+H2SO4 =Na2SO4+H2O+CO2↑;(3)打开K3 ,将分液漏斗中稀硫酸放入广口瓶中,将燃着的木条放在管口,木条熄灭,关闭K3,打开K4
【考点精析】解答此题的关键在于理解二氧化碳的化学性质的相关知识,掌握化学性质:一般情况下不能燃烧,也不支持燃烧,不能供给呼吸;与水反应生成碳酸;能使澄清的石灰水变浑浊;与灼热的碳反应,以及对一氧化碳的性质的理解,了解一氧化碳的物理性质:无色,无味的气体,密度比空气略小,难溶于水;一氧化碳的化学性质:可燃性和还原性.