题目内容
【题目】请认真回忆物质与其构成粒子之间的关系,回答下列问题:
(1)金属铁是由 构成的,氯化钾是由 构成的,二氧化碳是由构成的.
(2)原子得到或失去电子后形成离子.某粒子的结构示意图为 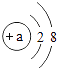
①当a=时,该粒子是原子,该原子位于元素周期表中第周期.
②当a=8时,该粒子是(填“原子”、“阳离子”或“阴离子”).
【答案】
(1)铁原子,氯离子、钾离子,二氧化碳分子构成的
(2)10,二,阴离子
【解析】(1)金属铁是由铁原子构成的,氯化钠是由钠离子和氯离子构成的,二氧化碳是由二氧化碳分子构成的;
(2)①在原子中,核内质子数=核外电子数,故a=2+8=10表示的是原子,核外有两个电子层,故位于第二周期;②当a=8时,该粒子的核内质子数<核外电子数,表示的是阴离子.
故答案为:(1)铁原子;氯离子、钾离子;二氧化碳分子构成的;(2)10;二;阴离子.
(1)金属由原子直接构成,盐类物质一般由离子构成,非金属氧化物由分子构成;
(2)①当质子数等于核外电子总数时是原子结构示意图,有几个电子层就在第几周期;
②当质子数大于核外电子总数时是阳离子,当质子数小于最外层电子总数时,是阴离子.

练习册系列答案
 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案
相关题目
【题目】将金属与金属(或非金属)加热熔合在一起就能形成合金.根据下列金属的熔点、沸点,其不能形成合金的是( )
Na | Cu | Al | Fe | |
熔点/℃ | 97.81 | 1083 | 660 | 1535 |
沸点/℃ | 882.9 | 2595 | 2467 | 3000 |
A. Cu NaB. Al FeC. Fe CuD. Al Na