题目内容
二氧化碳能使澄清石灰水变浑浊.王浩同学查阅资料发现:氢氧化钠溶液与氢氧化钙溶液性质十分相似,也能与二氧化碳发生反应,但此反应无明显实验现象,其反应的化学方程式为:CO2+2NaOH=Na2CO3+H2O.他为了能证明氢氧化钠溶液与二氧化碳确实发生了反应,设计了如下方案.请你将她设计的方案补充完整:
| 实验步骤和方法 | 现象 | 结论 | 启示 | |
| 方案 | 向一个软塑料瓶中充满二氧化碳,再注入少量氢氧化钠溶液,盖紧瓶盖,摇动塑料瓶. |
二氧化碳与氢氧化钠反应会使软塑料瓶内压强减小,瓶子变瘪,从而证明两者发生了反应.
故答案为:
故答案为:
| 实验步骤和方法 | 现象 | 结论 | 启示 | |
| 方案 | 向一个软塑料瓶中充满二氧化碳,再注入少量氢氧化钠溶液,盖紧瓶盖,摇动塑料瓶 | 塑料瓶变瘪 | 氢氧化钠与二氧化碳在溶液中发生了反应 | 从反应物二氧化碳的减少(压强减小)来判断反应的发生 |

练习册系列答案
 全优点练单元计划系列答案
全优点练单元计划系列答案
相关题目
小苏打(NaHCO3)是一种重要的盐类物质,在食品和医药工业中用途很广.小茹与小艺同学为探究小苏打的性质,进行了猜想,并设计实验进行验证.请你帮助她们将下列实验报告填写完整,并参与她们的探究.
实验反思:
小茹认为探究小苏打加热分解的实验装置有一处错误,请指出错误 .
继续探究1:
经查:NaHCO3在溶液中主要解离成Na+、HCO3-.HCO3-与OH-反应生成水和CO32-.
猜想三中NaHCO3溶液与澄清石灰水反应的产物是什么?
有以下的猜想,你认为NaHCO3溶液与澄清石灰水反应不可能生成的物质是 (填序号).
①CaCO3 ②NaOH ③H2O ④CO2
通过实验可确定其他物质为生成物.
继续探究2:
猜想四中小苏打受热分解所得白色固体成分是什么?
小茹猜想:是NaOH
小茹验证:取少量白色固体,加水溶解,滴入酚酞溶液,溶液变红色.
小茹结论:水溶液显碱性,说明白色固体是NaOH.
小艺猜想:是Na2CO3.
小艺验证:取少量白色固体加入试管中,滴入盐酸,产生能使澄清石灰水变浑浊的气体.
小艺结论:白色固体是Na2CO3.
正确推理:
小苏打受热发生反应的化学方程式为: .另一同学根据实验所得结论错误的原因是 .
| 猜想 | 实验操作 | 实验现象 | 结论(或化学方程式) |
| 猜想一:NaHCO3溶液显碱性 | 取NaHCO3固体加入试管中,加适量水溶解并滴入2-3滴酚酞试液,振荡 | 溶液变成浅红色 | 溶液显碱性 |
| 猜想二:能与酸反应 | 取少量NaHCO3固体加入试管中,滴加稀盐酸 | 化学方程式: | |
| 猜想三:能与碱反应 | 取少量NaHCO3固体加适量水溶解,向溶液中加入澄清石灰水 | 出现白色沉淀 | NaHCO3溶液能与碱反应 |
| 猜想四:加热能分解 | 取适量NaHCO3固体加入试管中,如下图所示加热,产生的气体通入澄清石灰水中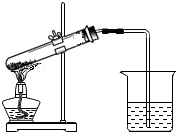 |
有气体产生,试管口部有水珠出现, |
NaHCO3固体受热分解有二氧化碳气体和水产生 |
小茹认为探究小苏打加热分解的实验装置有一处错误,请指出错误
继续探究1:
经查:NaHCO3在溶液中主要解离成Na+、HCO3-.HCO3-与OH-反应生成水和CO32-.
猜想三中NaHCO3溶液与澄清石灰水反应的产物是什么?
有以下的猜想,你认为NaHCO3溶液与澄清石灰水反应不可能生成的物质是
①CaCO3 ②NaOH ③H2O ④CO2
通过实验可确定其他物质为生成物.
继续探究2:
猜想四中小苏打受热分解所得白色固体成分是什么?
小茹猜想:是NaOH
小茹验证:取少量白色固体,加水溶解,滴入酚酞溶液,溶液变红色.
小茹结论:水溶液显碱性,说明白色固体是NaOH.
小艺猜想:是Na2CO3.
小艺验证:取少量白色固体加入试管中,滴入盐酸,产生能使澄清石灰水变浑浊的气体.
小艺结论:白色固体是Na2CO3.
正确推理:
小苏打受热发生反应的化学方程式为:
