题目内容
将24.5克氯酸钾和4.5克二氧化锰混合后放入试管充分加热后,试管中剩余的固体质量为
- A.19.4克
- B.20克
- C.14.9克
- D.4.5克
A
分析:根据氯酸钾受热分解后固体质量是减去生成气体的质量即可.
解答:设24.5克氯酸钾完全分解生成氧气质量为X.则:
2KClO3 2KCl+3O2↑
2KCl+3O2↑
245 96
24.5g X
根据: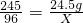 解得:X=9.6g
解得:X=9.6g
试管中剩余的固体质量为24.5g+4.5g-9.6g=19.4g
故答案为:19.4g.
点评:解答本题关键是根据参加反应的氯化钾的质量算出氧气的质量;根据剩余固体质量要减去生成的氧气的质量.
分析:根据氯酸钾受热分解后固体质量是减去生成气体的质量即可.
解答:设24.5克氯酸钾完全分解生成氧气质量为X.则:
2KClO3
 2KCl+3O2↑
2KCl+3O2↑245 96
24.5g X
根据:
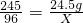 解得:X=9.6g
解得:X=9.6g试管中剩余的固体质量为24.5g+4.5g-9.6g=19.4g
故答案为:19.4g.
点评:解答本题关键是根据参加反应的氯化钾的质量算出氧气的质量;根据剩余固体质量要减去生成的氧气的质量.

练习册系列答案
 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案
相关题目