题目内容
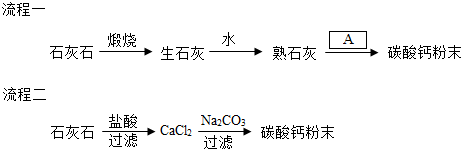
石灰石是生产石灰、水泥的主要原料.某兴趣小组摸仿化验室测定石灰石样品中碳酸钙的质量分数,进行了以下实验(假设杂质不参加反应):称取石灰石样品12g放入烧杯中;慢慢加入稀盐酸,不断搅拌,至不发生气泡为上,称得消耗稀盐酸73g;称量反应后烧杯中剩余物的质量为80.6g.试根据实验数据计算石灰石样品中碳钙的质量分数.
解:(1)根据质量守恒定律,二氧化碳的质量为:73g+12g-80.6g=4.4g.
(2)设该石灰石样品中碳酸钙的质量为x.
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 4.4g
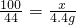
解之得:x=10g
此石灰石中碳酸钙的质量分数为: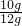 ×100%≈83.3%
×100%≈83.3%
答:该石灰石样品中碳酸钙的质量分数为83.3%.
分析:(1)根据质量守恒定律可知:反应后比反应前减少的质量是生成二氧化碳的质量;
(2)根据化学方程式由二氧化碳的质量可以计算出石灰石中碳酸钙的质量,进而计算出石灰石中碳酸钙的质量分数.
点评:本题主要考查有关化学方程式的计算和质量分数的计算,难度较小.
(2)设该石灰石样品中碳酸钙的质量为x.
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 4.4g
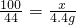
解之得:x=10g
此石灰石中碳酸钙的质量分数为:
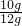 ×100%≈83.3%
×100%≈83.3%答:该石灰石样品中碳酸钙的质量分数为83.3%.
分析:(1)根据质量守恒定律可知:反应后比反应前减少的质量是生成二氧化碳的质量;
(2)根据化学方程式由二氧化碳的质量可以计算出石灰石中碳酸钙的质量,进而计算出石灰石中碳酸钙的质量分数.
点评:本题主要考查有关化学方程式的计算和质量分数的计算,难度较小.

练习册系列答案
 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案
相关题目
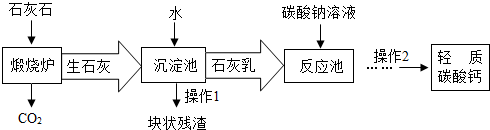
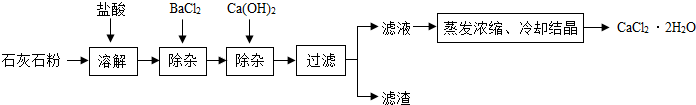
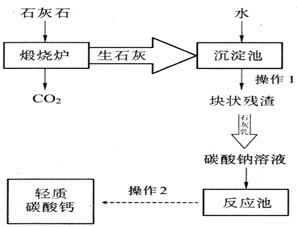 碳酸钙的新用途
碳酸钙的新用途