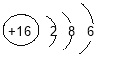题目内容
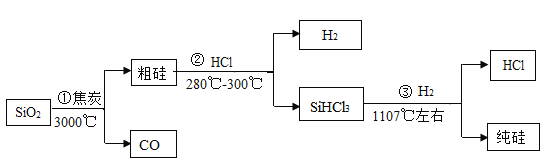
【题目】中国芯彰显中国“智”造,芯片的基材主要是高纯硅(Si),工业上生产高纯硅的流程如下,请回答下列问题:
(1)二氧化硅中硅元素化合价为_____。
(2)反应①的化学方程式为_____,该反应体现出焦炭的_____性。
(3)该流程中可循环利用的物质是_____(填物质名称,写一种即可)。
【答案】+4 SiO2+2C![]() Si+2CO↑ 还原 氯化氢或氢气
Si+2CO↑ 还原 氯化氢或氢气
【解析】
(1)二氧化硅(SiO2)中,氧元素显-2价,根据化合物中各元素的化合价代数和为零可知,硅元素化合价为+4价;
(2)根据流程图可知,反应①是碳与二氧化硅在3000℃时反应生成硅和一氧化碳,反应的化学方程式为SiO2+2C![]() Si+2CO↑,碳在反应中得到氧元素,该反应体现出焦炭的还原性。
Si+2CO↑,碳在反应中得到氧元素,该反应体现出焦炭的还原性。
(3)该流程中,氯化氢和氢气既是反应物又是生成物,可循环利用的物质是氯化氢或氢气。

 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案【题目】小意同学对所学化学知识进行归纳整理,你认为有错误的是![]()
![]()
A物质的性质 | B能源与燃料 |
①有可燃性的气体是: ②所有的金属都是银白色的固体 ③所有的化学反应都是放热的 | ①水既是资源、也是能源,但不是燃料 |
C合金与纯金属 | D化学之最 |
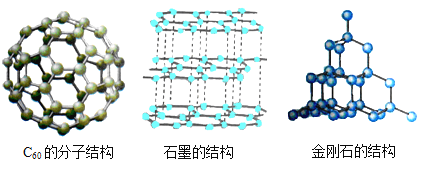
①1角、5角、1元的硬币均为合金 ②合金的硬度比其组成纯金属高 ③合金的熔点比其组成纯金属低 | ①自然界最轻的物质是氢气 ②自然界最硬的物质是金刚石 ③空气中含量最多的物质是氮气 |
A.AB.BC.CD.D
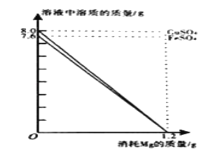
【题目】(演示实验)将一定量稀硫酸加入盛有氢氧化钠溶液的容器内,并不断搅拌。两者发生反应的化学方程式为________。
(提出问题)反应后溶液中溶质的成分是什么?
(猜想假设)甲组同学的猜想如下:
猜想I:只有Na2SO4;
猜想Ⅱ:有_________;
猜想Ⅲ:有Na2SO4和NaOH;
猜想Ⅳ:有Na2SO4、H2SO4和NaOH。
乙组同学对以上猜想提出质疑,认为猜想V不合理,其理由是___________。
(查阅资料)
①Na2SO4溶液显中性。
②![]() 、
、![]()
(实验探究)为了验证其余的猜想,各小组分别按照下列三个实验方案进行探究。
实验方案 | 实验现象 | 实验结论 |
①取样,滴入紫色石蕊试液 | ___________ | 溶液中含有NaOH |
②取样,滴加CuSO4溶液 | ___________ | |
③取样,滴加BaCl2溶液 | 产生白色沉淀 | 溶液中含有H2SO4 |
(得出结论)在老师指导下,同学们一致确定猜想Ⅲ成立。
(评价反思)
(1)丙组同学认为滴加BaCl2溶液产生白色沉淀,并不能证明溶液中一定含有H2SO4,因为________。
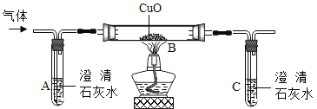
(2)若要证明反应后的溶液中含有H2SO4,可以选择的试剂是________(填字母)。
A 酚酞试液 B pH试纸 C CuO D 铜片