题目内容
【提出问题】该厂附近所降雨水是否是酸雨?空气里SO2是否超标呢?【查阅资料】Ⅰ.我国关于SO2在风景区、居民区、工厂区的空气质量最高标准分别见下表:
| 级 别 | Ⅰ | Ⅱ | Ⅲ |
| SO2一小时测定平均含量(mg/m3) | 0.15 | 0.5 | 0.7 |
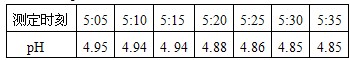
【设计实验1】第一组同学取刚降到地面的雨水水样,用pH计(测pH的仪器)每隔几分钟测一次pH,其数据如下表所示:
| 测定时刻 | 5:05 | 5:10 | 5:15 | 5:20 | 5:25 | 5:30 | 5:35 |
| pH | 4.95 | 4.95 | 4.91 | 4.88 | 4.86 | 4.85 | 4.85 |
【设计实验2】第二小组同学设计以下步骤来测定空气中SO2的含量.
(1)用2L的空可乐瓶采集工厂附近的空气样品.采样的具体操作是:
(2)向取回的装有2L空气样品的可乐瓶中加入NaOH溶液(假设在加入溶液的过程中,瓶中气体不会向外逸出),盖紧瓶塞后充分振荡.仿照CO2与NaOH溶液的反应,写出SO2与NaOH溶液反应的化学方程式:
(3)加入一定量氧化剂H2O2,使其中Na2SO3完全转化为Na2SO4.向可乐瓶中加入过量的BaCl2溶液.Na2SO4和BaCl2反应的化学方程式为:
(4)经过过滤、洗涤、烘干,称量固体质量为1.165mg.
计算:1.165mg硫酸钡中硫元素的质量为
由质量守恒定律可知,2L空气样品中SO2的质量为
由空气质量标准可得出结论:该厂排放的SO2严重超标.
【发现新问题】考虑到空气中的各种气体成分,第一组认为第二组同学的SO2的含量偏大,其依据是
你提出的实验改进方案是
【反思与应用】为尽快改善该地区的空气质量,请你提出一条合理化建议:
分析:PH<5.6的雨水称为酸雨.根据反应物和生成物及其质量守恒定律可以正确的书写化学方程式.硫酸钡的质量乘以硫酸钡中硫元素的质量分数可得硫元素的质量,进而可以求出二氧化硫的质量.空气中的二氧化碳和氢氧化钠反应生产的碳酸钠也能和氯化钡反应生成碳酸钡沉淀,碳酸钡沉淀能和稀硝酸反应从而使得沉淀溶解.工厂废气处理后再排放能够改善空气质量.
解答:解:【设计实验1】雨水的PH<5.6,属于酸雨.故填:是.
【设计实验2】
(1)采集空气样品的方法是:可乐瓶装满水盖上瓶盖拿到工厂附近,然后倒掉水,擦干,再盖上瓶盖.
(2)二氧化硫和氢氧化钠反应生成亚硫酸钠和水,反应的化学方程式为:SO2+2NaOH═Na2SO3+H2O.
(3)氯化钡和硫酸钠反应能生成硫酸钡沉淀和氯化钠,反应的化学方程式为:BaCl2+Na2SO4═BaSO4↓+2NaCl.
(4)1.165mg硫酸钡中硫元素的质量为:1.165mg×
×100%=0.16mg.故填:0.16.
由质量守恒定律可知,2L空气样品中SO2的质量为:0.16mg÷50%=0.32mg.故填:0.32.
【发现新问题】第二组同学的SO2的含量偏大的原因是:空气中的二氧化碳也要和氢氧化钠溶液反应,反应后生成的碳酸钠要和BaCl2溶液反应,生成碳酸钡沉淀;
实验改进方案是:向沉淀中加入过量的稀硝酸后,再进行其余操作.
【反思与应用】工厂废气进行治理,达标后再排放有利于改善空气质量.故填:工厂废气进行治理,达标后再排放.
【设计实验2】
(1)采集空气样品的方法是:可乐瓶装满水盖上瓶盖拿到工厂附近,然后倒掉水,擦干,再盖上瓶盖.
(2)二氧化硫和氢氧化钠反应生成亚硫酸钠和水,反应的化学方程式为:SO2+2NaOH═Na2SO3+H2O.
(3)氯化钡和硫酸钠反应能生成硫酸钡沉淀和氯化钠,反应的化学方程式为:BaCl2+Na2SO4═BaSO4↓+2NaCl.
(4)1.165mg硫酸钡中硫元素的质量为:1.165mg×
| 32 |
| 233 |
由质量守恒定律可知,2L空气样品中SO2的质量为:0.16mg÷50%=0.32mg.故填:0.32.
【发现新问题】第二组同学的SO2的含量偏大的原因是:空气中的二氧化碳也要和氢氧化钠溶液反应,反应后生成的碳酸钠要和BaCl2溶液反应,生成碳酸钡沉淀;
实验改进方案是:向沉淀中加入过量的稀硝酸后,再进行其余操作.
【反思与应用】工厂废气进行治理,达标后再排放有利于改善空气质量.故填:工厂废气进行治理,达标后再排放.
点评:解答本题要充分理解酸雨的含义,掌握化学方程式的书写方法,掌握相关方面的计算方法,只有这样才能对问题做出正确的判断.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
【提出问题】该厂附近所降雨水是否是酸雨?空气里SO2是否超标呢?
【查阅资料】Ⅰ.我国关于SO2在风景区、居民区、工厂区的空气质量最高标准分别见下表:
| 级 别 | Ⅰ | Ⅱ | Ⅲ |
| SO2一小时测定平均含量(mg/m3) | 0.15 | 0.5 | 0.7 |
【设计实验1】第一组同学取刚降到地面的雨水水样,用pH计(测pH的仪器)每隔几分钟测一次pH,其数据如下表所示:
| 测定时刻 | 5:05 | 5:10 | 5:15 | 5:20 | 5:25 | 5:30 | 5:35 |
| pH | 4.95 | 4.95 | 4.91 | 4.88 | 4.86 | 4.85 | 4.85 |
【设计实验2】第二小组同学设计以下步骤来测定空气中SO2的含量.
(1)用2L的空可乐瓶采集工厂附近的空气样品.采样的具体操作是:________.
(2)向取回的装有2L空气样品的可乐瓶中加入NaOH溶液(假设在加入溶液的过程中,瓶中气体不会向外逸出),盖紧瓶塞后充分振荡.仿照CO2与NaOH溶液的反应,写出SO2与NaOH溶液反应的化学方程式:________.
(3)加入一定量氧化剂H2O2,使其中Na2SO3完全转化为Na2SO4.向可乐瓶中加入过量的BaCl2溶液.Na2SO4和BaCl2反应的化学方程式为:________.
(4)经过过滤、洗涤、烘干,称量固体质量为1.165mg.
计算:1.165mg硫酸钡中硫元素的质量为________mg.
由质量守恒定律可知,2L空气样品中SO2的质量为________mg.
由空气质量标准可得出结论:该厂排放的SO2严重超标.
【发现新问题】考虑到空气中的各种气体成分,第一组认为第二组同学的SO2的含量偏大,其依据是________;
你提出的实验改进方案是________.
【反思与应用】为尽快改善该地区的空气质量,请你提出一条合理化建议:________.