题目内容
【题目】结合如图实验回答问题: 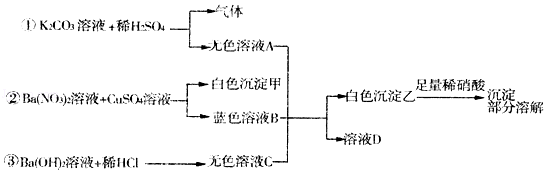
(1)写出反应③的化学方程式;
(2)溶液D的颜色是 , 白色沉淀乙的组成是;
(3)下列说法正确的是;
A.溶液A可以做植物营养液
B.溶液B中的阳离子可能有两种
C.确定溶液C中溶质成分需要借助酸碱指示剂
(4)写出溶液D中一定存在的离子的符号 .
【答案】
(1)Ba(OH)2+2HCl=BaCl2+2H2O
(2)蓝色;硫酸钡、碳酸钡
(3)AB
(4)K+、Cu2+、Cl﹣、NO3-
【解析】解:碳酸钾和硫酸反应生成硫酸钾、水和二氧化碳,所以无色溶液A中一定含有硫酸钾,可能含有硫酸、碳酸钾中的一种,硝酸钡和硫酸铜反应生成硫酸钡沉淀和硝酸铜,所以甲是硫酸钡沉淀,B中一定含有硝酸铜,可能含有硝酸钡、硫酸铜中的一种,氢氧化钡和盐酸反应生成氯化钡和水,所以C中一定含有氯化钡,可能含有氢氧化钡、盐酸中的一种,A、B、C三种溶液混合,生成部分溶于酸的白色沉淀乙和溶液D,所以A中含有硫酸钾、碳酸钾,B中含有硝酸铜、硝酸钡,C中含有氯化钡,所以(1)反应③是氢氧化钡和盐酸反应生成氯化钡和水,化学方程式为:Ba(OH)2+2HCl=BaCl2+2H2O;(2)通过推导可知,溶液D的颜色是蓝色,白色沉淀乙的组成是:碳酸钡、硫酸钡;(3)A.溶液A中含有碳酸钾、硫酸钾,可以做植物营养液,故A正确; B.溶液B中的阳离子可能有钡离子、铜离子两种,故B正确;
C.三种溶液混合后,没有气体生成,没有生成蓝色沉淀,所以溶液C中溶质成分遇到不含氯化氢、氢氧化钡,不需要借助酸碱指示剂,故C错误;
故选:AB;(4)碳酸钾和钡离子反应生成碳酸钡沉淀,硫酸钾和钡离子反应生成硫酸钡沉淀,铜离子不会生成沉淀,所以溶液D中一定存在的离子的符号:K+、Cu2+、Cl﹣、NO3- .
所以答案是:(1)Ba(OH)2+2HCl=BaCl2+2H2O;(2)蓝色,碳酸钡、硫酸钡;(3)AB;(4)K+、Cu2+、Cl﹣、NO3- .
【考点精析】关于本题考查的书写化学方程式、文字表达式、电离方程式,需要了解注意:a、配平 b、条件 c、箭号才能得出正确答案.